
shotshop.com
Die Titration ist ein Verfahren, mit dem sich die Konzentration einer chemischen Substanz in einer Lösung bestimmen lässt.
Die Titration ist ein Verfahren, mit dem sich die Konzentration einer chemischen Substanz in einer Lösung bestimmen lässt, zum Beispiel die Konzentration von Salzsäure oder Natronlauge.
Wie funktioniert eine Titration? Das „Klassenraum-Fußball-Modell“
Das Verfahren der Titration ist einfach und präzise. Wie es funktioniert, zeigt das „Klassenraum-Fußball-Modell“:
Nehmen wir an, Du willst herausfinden, wie viele Kinder sich in einem Klassenraum befinden, die sehr gerne Fußball spielen. Dafür darfst Du aber nicht fragen oder in den Raum hineingehen. Stattdessen rollst Du durch die geöffnete Tür Fußbälle in den Klassenraum. Einen nach dem anderen.
Befindet sich ein „Fußballkind“ im Klassenraum, das keinen Ball hat, dann schnappt es sich den Fußball und dribbelt damit herum. Wenn alle Fußballkinder einen Ball haben, dann rollen die nächsten Bälle einfach zur gegenüberliegenden Tür wieder heraus, weil die übrigen Kinder kein Interesse an den Bällen zeigen. Die Antwort auf die Ursprungsfrage ist nun ganz einfach: Es sind so viele Fußballkinder im Raum, wie Bälle darin verschwunden sind.
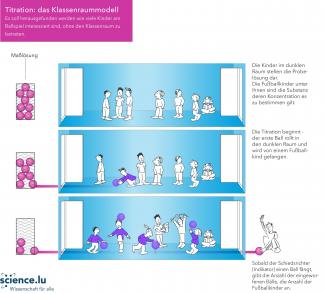
Hier kannst Du das "Klassenraum-Fußball-Modell"-Schema im PDF-Format herunterladen.
Maßlösung und Probelösung
In der Chemie werden die Fußbälle und die Kinder ersetzt durch zwei Substanzen, die miteinander eine chemische Reaktion eingehen – analog dem Auffangen der Bälle durch die Kinder. Die Fußbälle bilden die „Maßlösung“ (die wir genau kennen), die Kinder die „Probelösung“ (bei welcher wir herausfinden möchten, in welcher Konzentration sie unsere Substanz enthält).
Nach und nach wird die Maßlösung in die Probelösung getropft. Was für eine Maßlösung man verwendet, hängt von der Substanz in der Probelösung ab. Um die Konzentration der Probelösung „Salzsäure“ zu bestimmen, braucht man eine andere Maßlösung als zur Konzentrationsbestimmung der Probelösung „Natronlauge“.
Versuchsaufbau und –Ablauf.
Der Versuchsaufbau bei der Titration ist meist so, dass an einem Stativ eine Bürette (das ist ein dünnes Glasrohr mit einer Volumenskala und einem Verschlusshahn am unteren Ende) angebracht ist. Darunter befindet sich ein Erlenmeyerkolben oder ein Becherglas. In der Bürette befindet sich die Maßlösung, im Glas darunter die Probelösung. Die Probelösung enthält einen Indikator, zum Beispiel einen Farbstoff. Durch plötzliche Farbveränderung zeigt er an, wenn die chemische Reaktion vollständig abgelaufen ist („alle fußballbegeisterten Kinder haben einen Fußball!“)
Öffnet man den Hahn der Bürette, dann läuft die Maßlösung langsam in das Glas mit der Probelösung. Den Inhalt des Glases muss man dabei fortlaufend beobachten – damit man die Farbveränderung des Indikators sofort sieht. Dann ist nämlich die chemische Reaktion vollständig abgelaufen, man verschließt den Hahn und liest ab, wie viel der Maßlösung für die Reaktion notwendig war. Die Probelösung muss ständig umgerührt werden (manuell oder z.B. mit einem Magnetrührer, damit die Maßlösung gleichmäßig in der Probelösung verteilt werden kann).

Hier kannst Du das Titration-Schema im PDF-Format herunterladen.
Ein konkretes Beispiel aus der Praxis
Du willst die Konzentration einer Essig-Wasser-Mischung bestimmen. Dazu versetzt Du die Essiglösung mit dem Farbstoff Phenolphthalein. Diese Probelösung ist zunächst durchsichtig. Du gibst genau 100 ml Essig-Wasser-Mischung in dein Becherglas.
In Deine Bürette füllst Du Natronlauge einer bekannten Konzentration (z. B. 0,1-molar, d. h. 0,1 Einheiten „normalisierter“ Natronlauge pro Liter Wasser – kann man fertig kaufen oder selbst mit Natron anmischen. Vorsicht, ätzend! Augenschutz tragen!).
Nun beginnt die Titration, indem Du die Maßlösung (Natronlauge) in die Probelösung (Essigsäure) fließen lässt. In dem Moment, in dem die Natronlauge die Säure vollständig neutralisiert hat, färbt das Phenolphtalein die Lösung rosa.
Schließe den Hahn der Bürette und lese ab, wie viel Natronlauge Du benutzt hast. Wenn Du jetzt diese Menge durch das Volumen der Probelösung teilst und mit der Konzentration 0,1 Mol pro Liter multiplizieren (Dreisatz), dann erhältst Du die gesuchte Essigkonzentration. Ein Beispiel: Nachdem Du 25ml 0,1-molare Natronlauge in die Essiglösung (100ml Volumen) getropft hast, schlägt die Farbe um. Deine Essiglösung ist dann 100ml/25ml*0,1-molar, also 0,4-molar.
Du möchtest bestimmen, wieviel Vitamin C in deinem Apfel enthalten ist? Dann schau dir diese Experimentbeschreibung an:
Autor: scienceRELATION
Editor: Michelle Schaltz (FNR)







