scienceRELATIONS
Prof. Michael Heneka, Direktor des Luxembourg Center for Systems Biomedicine (LCSB) an der Universität Luxemburg.
In Luxemburg leben geschätzt rund 9000 Menschen mit Demenzerkrankungen, der Großteil davon mit der Alzheimer-Krankheit. Die Demenz vom Typ Alzheimer wurde nach dem deutschen Neurologen Alois Alzheimer benannt, der die Symptome Anfang des 20. Jahrhunderts erstmals beschrieb. Die genauen Ursachen für die Entstehung sind jedoch bis heute nicht völlig geklärt. Weltweit arbeiten Forscherinnen und Forscher an Therapieansätzen, um die Krankheit des Vergessens zu lindern oder sogar heilen zu können. Was die Wissenschaft über die Entstehung von Alzheimer weiß, welche Therapien es gibt, welche Forschungsansätze Hoffnung machen und was jeder Einzelne zur Vorbeugung tun kann, erklärt der Experte für neurodegenerative Erkrankungen Michael Heneka vom interdisziplinären Zentrum LCSB der Universität Luxemburg.
Viele ältere Menschen fürchten sich vor der Alzheimer-Krankheit. Aber was genau ist Alzheimer – worin unterscheidet sich diese Krankheit von normaler altersbedingter Vergesslichkeit und anderen Demenzerkrankungen?
Michael Heneka: Morbus Alzheimer ist eine neurodegenerative Erkrankung, also eine Erkrankung des Nervensystems. Bei den Betroffenen kommt es zu Eiweißablagerungen im Gehirn, die Nervenzellen absterben lassen und zum geistigen Abbau führen. Zu Beginn zeigt sich die Krankheit in der überwiegenden Zahl der Fälle durch Störungen des Kurzzeitgedächtnisses. Das heißt, man kann sich an kurz zurückliegende Ereignisse nicht mehr erinnern. Später kommt es zum Verlust weiterer kognitiver Bereiche wie Sprache, Lesen, Rechnen, Visuokonstruktion – das ist die Fähigkeit, Muster oder Formen zu erkennen – und Organisation.
Damit unterscheidet sich die Alzheimer-Krankheit deutlich von der normalen Altersvergesslichkeit. Das normale Altern setzt zwar auch Prozesse im Körper in Gang, die die geistigen Fähigkeiten einschränken. Sie gehen aber nicht völlig verloren. Wenn einem gesunden Menschen mit fortschreitendem Alter zum Beispiel Rechnen oder Schreiben schwerer fällt, so kommt er in der Regel dennoch im Alltag zurecht und kann noch autonom leben. Alzheimerpatienten können dies nicht mehr.
Die Alzheimer-Krankheit ist die häufigste aller Demenzerkrankungen. Daneben sind vaskuläre, also gefäßbedingte Demenzen, die Lewy-Körperchen-Krankheit, die Demenz bei Morbus Parkinson sowie die Frontotemporale Demenz am häufigsten. Sie sind durch andere Symptome gekennzeichnet und haben andere biologische Ursachen z.B. andere Genmutationen oder andere Eiweißablagerungen.
Wie alt sind Menschen in der Regel, wenn sie die Diagnose „Alzheimer“ erhalten, und wie hoch ist dann noch ihre Lebenserwartung?
Die kognitiven Einschränkungen setzen meist zwischen dem 60. und 65. Lebensjahr ein und nehmen dann kontinuierlich zu. Je nachdem, in welchem Lebensalter sich die Krankheit zeigt, wirkt sie sich nicht nur auf die Lebensqualität aus, sondern auch auf die Lebenserwartung. In Europa und in den USA überleben Alzheimer-Patienten die Krankheit im Durchschnitt um etwa zwölf Jahre. Die Lebenserwartung hängt auch von den Lebensumständen, der Kultur und der Gesundheitsversorgung eines Landes ab und fällt deshalb je nach Land sehr unterschiedlich aus. Die Weltgesundheitsorganisation kann darum bis heute für Alzheimer-Patienten keine durchschnittliche Lebenserwartung beziffern, die weltweit gelten würde.
Die Krankheit wurde im Jahr 1907 erstmals beschrieben. Was weiß die Forschung heute über die Entstehung von Alzheimer?
Die Wissenschaft hat in den vergangenen 20 Jahren entdeckt, dass die Krankheit nicht erst mit ersten Auftreten von Gedächtnisstörungen im Alter beginnt, sondern 20 bis 30 Jahre zuvor. Alzheimer ist also keine Erkrankung des Alters. Die Erkrankung beginnt etwa im vierten Lebensjahrzehnt und ist damit eine Erkrankung des mittleren Lebensalters. Das Alter ist nicht, wie man oft liest, der größte Risikofaktor für die Alzheimer-Erkrankung selbst. Das Alter ist der Risikofaktor für das Auftreten von Symptomen. Denn dank der Kompensationsfähigkeit des Gehirns wird die Hirnfunktion erst viele Jahre später beeinträchtigt. In anderen Worten: Das Gehirn wird bereits geschädigt, lange bevor die ersten Symptome auftreten. Das ist bei der Parkinson-Krankheit ähnlich. Bis sich bei Parkinson die erste Bewegungsstörung bemerkbar macht, müssen 60 bis 70 Prozent der entsprechenden dopaminergen Nervenzellen verloren sein.
Was kann man tun, wenn Alzheimer schon im vierten Lebensjahrzehnt entsteht, aber unentdeckt bleibt?
Da Menschen ohne Symptome nicht zum Arzt gehen, befindet sich eine große Zahl von Menschen auf dem Weg in die Alzheimer-Krankheit, ohne es zu ahnen. Die Herausforderung für Forschung und Medizin ist es, die Vorstadien zu diagnostizieren und die Betroffenen früher zu identifizieren. Denn man kann tatsächlich früh Einfluss auf die Krankheit nehmen, und zwar vor allem durch gesunde Lebensführung. Heute leben weltweit etwa 44 Millionen Menschen mit Alzheimer, für das Jahr 2050 werden rund 150 Millionen Fälle erwartet. Würden die Menschen all die Ratschläge befolgen, deren Wirksamkeit wir heute schon kennen, könnte Schätzungen zufolge weltweit ein Drittel der Erkrankungen verhindert werden - das heißt bis zu 50 Millionen Fälle. Das ist eine mächtige Zahl, auch in gesundheitspolitischer Hinsicht: Wir müssen die Menschen früh für diese Lebensstilfaktoren sensibilisieren.
Sollte man sich als Vierzigjähriger schon auf Morbus Alzheimer testen lassen?
Derzeit eher nicht, da noch keine präventive Medikation zugelassen wurde. Doch jeder kann schon heute seinen Lebensstil individuell anpassen.
Was sind denn die goldenen Ratschläge für eine gesunde Lebensführung?
Ernähren Sie sich mediterran, bewegen Sie sich viel und regelmäßig, reduzieren sie hohen Blutdruck und Fettleibigkeit. In einer vielbeachteten Studie unter Leitung der kalifornischen Forscherin Rachel Whitmer wurde eine Kohorte junger Männer mit und ohne Übergewicht untersucht. 30 Jahre später hatten diejenigen mit deutlich erhöhtem Body-Mass-Index und Bauchumfang ein bis zu vierfach erhöhtes Risiko, an Alzheimer zu erkranken. Außerdem sollten Sie auf Nikotin und Alkohol verzichten, systemische Entzündungen wie etwa eine Lungenentzündung konsequent behandeln lassen und Kopftraumata vermeiden. Tragen Sie immer einen Helm beim Radfahren.
Infobox
Wenn jemand mit Gedächtnisproblemen zum Arzt kommt, ist die Wahrscheinlichkeit für eine Demenzerkrankung bereits hoch. Bei etwa 20 Prozent der Fälle steckt jedoch etwas ganz anderes dahinter, das sich als Gedächtnisstörung äußert. Dazu gehören der Normaldruckhydrocephalus aufgrund einer Ansammlung von Flüssigkeit im Gehirn, Schilddrüsenerkrankungen, hormonelle Veränderungen oder Veränderungen, die Blutgefäße und die Blutversorgung des Gehirns betreffen. Diese Veränderungen imitieren das Bild einer Demenz, sind aber zu fast hundert Prozent heilbar.
Zur Diagnose sollte bei jedem Patienten mit Hilfe der Kernspintomographie ein Bild des Gehirns gemacht werden. Das erlaubt es, die Binnenstruktur und das Gewebe des Gehirns wirklich beurteilen zu können. Zu den weiteren Untersuchungen zählen eine Doppler- und eine Duplex-Sonographie, um die Versorgung der Blutgefäße im Hirn zu prüfen, ein Elektroenzephalogramm, das die elektrische Aktivität des Gehirns misst, eine Nervenwasseruntersuchung und eine Blutanalyse zur funktionellen Untersuchung von Organen wie Herz, Leber oder Niere im klinisch-chemischen Labor. Denn auch beeinträchtigte Organe können sich auf die geistige Leistung auswirken.
Dann wird im Nervenwasser nach bestimmten Eiweißen gesucht, die mit neurodegenerativen Erkrankungen assoziiert werden. Anhand dieser Eiweiße lässt sich abschätzen, um was für eine Demenzerkrankung es sich wahrscheinlich handelt. Dieser Teil kann dem Experten zufolge in Zukunft eventuell durch einen neuartigen Bluttest ersetzt werden. Dieser erkennt eine Veränderung des Tau-Eiweißes, die in Zusammenhang mit der Alzheimer-Krankheit steht, in 98 Prozent der Fälle. Alzheimer lässt sich also gut diagnostizieren, auch wenn es zu Beginn schwierig sein mag, die Krankheit von anderen Demenzerkrankungen klar zu trennen.
Zurück zu den Ursachen: Welche Rolle spielen die Gene?
Etwa fünf Prozent der Fälle sind auf direkte familiäre Vererbung zurückzuführen. Liegt bei Mutter oder Vater eine Mutation bestimmter Alzheimer-Gene (APP, PSEN1, PSEN2) vor, erben die Kinder das mutierte Gen mit einer Wahrscheinlichkeit von 50 Prozent. Wer es erbt, wird später an Alzheimer erkranken. Darüber hinaus tragen etwa zehn bis 15 Prozent der Bevölkerung ein Risikogen für nachlassende kognitive Leistung nach dem 60. Lebensjahr in sich, das ApoE4. Das ist eine hohe Zahl. Dennoch wird eine genetische Testung derzeit nur für Familien empfohlen, bei denen sich in jeder Generation eine deutliche Häufung der Fälle findet. Diese Empfehlung mag sich je nach Verfügbarkeit wirksamer Medikamente rasch ändern.
Über die letzten zwei Dekaden haben Forscher eine Anzahl weiterer Gene entdeckt, die das Alzheimerrisiko beeinflussen und die verschiedene biologische Prozesse beeinflussen. Davon sind chronische Entzündungen die häufigste. Alzheimer entsteht nach heutigem Forschungsstand demnach in den meisten Fällen durch das Zusammenspiel von genetischem Hintergrund, Entzündungen, Infektionen sowie dem persönlichem Lebensstil, aber auch Kopftraumata, etwa durch Fußballspiel oder Stürze. Und zumindest seinen Lebensstil kann jeder Einzelne selbst beeinflussen.
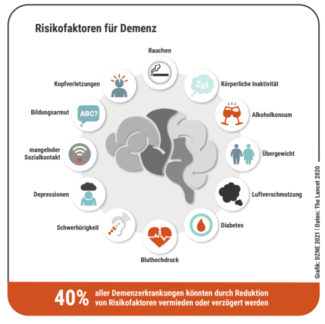
Quelle: Deutsches Zentrum für Neurodegenerative Erkrankungen
In manchen Studien wurden Umwelteinflüsse wie z.B. Aluminium oder auch Zahnfleischentzündungen mit dem Alzheimerrisiko in Verbindung gebracht.
Aluminium ist aus wissenschaftlicher Sicht nicht als Risiko identifiziert, das ist eher den Legenden zuzuordnen. Paradontitis ist eine Entzündung und damit ein Risikofaktor. Auch Hörverlust wurde als Risikofaktor beschrieben, könnte aber auch Symptom oder Folge sein.
Wenn die Diagnose feststeht – wie wird dann behandelt? Welche Fortschritte hat die Therapie gemacht?
Die Wissenschaft hat sich in den vergangenen 30 Jahren auf viele unterschiedliche Ansätze gestürzt. Ein Schwerpunkt ist, die pathologischen Merkmale der Krankheit zu verändern. Wir wissen aus den Untersuchungen von Gehirnen verstorbener Alzheimer-Patienten, dass sich im Gehirn der Betroffenen bestimmte Eiweiße ablagern: Amyloid-beta und Tau. Die Ablagerungen bilden sich sowohl zwischen als auch innerhalb der Nervenzellen und führen zu Entzündungen. Alle drei Faktoren tragen zum Absterben der Nervenzellen im Gehirn bei. Die Forschung versucht, diese Eiweiß-Ablagerungen durch Wirkstoffe aufzulösen. Ein neuer Therapieansatz ist die Therapie mit Antikörpern. Dabei geht es um eine passive Immunisierung, die den Körper dazu bringen soll, die schädlichen Eiweiße selbst abzubauen. In den USA sind entsprechende Medikamente bereits zugelassen und in Anwendung.
Werden sie auch in Europa bald zugelassen?
In der Europäischen Union wurde der Zulassungsantrag für zwei Antikörper-Medikamente abgelehnt. Auch die Behörden in Großbritannien haben kürzlich entschieden, dass die Antikörpertherapie zwar effektiv, aber im Vergleich zur Wirkung zu teuer ist, und den Antrag abgelehnt. Ein drittes Antikörpermedikament befindet sich zurzeit im Zulassungsprozess – man darf auf die Resultate und die Reaktionen in den USA und in Europa gespannt sein.
Ist die Behandlung mit Antikörpern ein entscheidender Durchbruch?
Nein, die Antikörper-Medikamente sind aus meiner Sicht keine „Gamechanger“. Sie stoppen und heilen die Erkrankung nicht, sondern verzögern das Fortschreiten einer bestimmten Pathologie und der geistigen Beeinträchtigung. Allerdings sollte man diesen neuen Therapieansatz auf faire Weise mit der Einführung neuer Medikamente bei anderen Krankheiten vergleichen. Hätten wir ähnlich wirksame Medikamente zum Beispiel gegen die Amyotrophe Lateralsklerose (ALS) oder besonders dramatische Tumorarten, wären wir überglücklich. Auch die ersten Chemotherapien für Krebskranke in den 60er-Jahren hatten starke Nebenwirkungen, waren gefährlich und teuer. Doch die Wissenschaft hat daraus gelernt und kann dank dieser Erfahrungen manche Tumore heute komplett ausheilen.
Auch mit der Antikörpertherapie stehen wir nun am Beginn. Die Medizin braucht die Chance, diesen ersten Schritt zu wagen. Irgendwann wird man dann verschiedene Behandlungen miteinander kombinieren können und bessere Wirkungen erzielen. Doch es scheint, dass Therapien von Demenzerkrankungen kritischer geprüft werden. Ich habe nun gemeinsam mit Kollegen zur Antikörpertherapie Stellung genommen; unsere Publikation wird bald im Fachblatt The Lancet erscheinen.
Erwarten Sie denn einen baldigen Forschungsdurchbruch?
Ein absoluter Durchbruch wurde schon zu häufig verkündet, so dass ich selbst eher mit einem stetigen Zuwachs an Wissen und therapeutischen Ansatzpunkten über die kommenden Jahre rechne. Neben wirkungsvollen Therapien werden wir auch weiter Biomarker entwickeln müssen, die uns anzeigen, welche Therapie zu welchem Zeitpunkt besonders wichtig und geeignet ist.
Mit welchen Medikamenten werden Patienten in Europa heute behandelt?
Es gibt in Europa zugelassene, gut wirksame symptomatische Medikamente. Sie wirken also nicht gegen die Ursachen der Krankheit, lindern aber die Symptome. Das ist möglich, in dem sie einerseits die Anwesenheit eines wichtigen Nervenbotenstoffes erhöhen und andererseits die toxische Wirkung bestimmter überstimulierter Rezeptoren blockieren. Richtig eingesetzt und kombiniert, können diese Medikamente bis zu drei Jahre lang wirken, die Symptome deutlich lindern und den Krankheitsverlauf verzögern. Das ist für die Betroffenen sehr viel. Sie zeigen dann weniger Funktionsstörungen, verwechseln seltener Dinge und orientieren sich besser. Leider werden viele Patienten nicht adäquat behandelt, weil viele Ärzte davon ausgehen, dass man gegen Alzheimer sowieso nichts ausrichten kann. Dem ist aber nicht so.
Andere vielversprechende Therapieansätze setzen auf Antikörper gegen Tau-Proteine sowie auf Therapien, die Entzündungen blockieren – an dieser Forschung ist auch das Luxembourg Centre for Systems Biomedicine beteiligt.
Auf welche Ansätze konzentriert sich die Alzheimerforschung am LCSB?
Kerngeschäft unserer Forschungsgruppe ist es, die entzündliche Komponente neurodegenerativer Krankheiten zu erforschen. Eine aktuelle Studie zusammen mit Forschern des Universitätsklinikums Bonn sowie Wissenschaftlern aus Frankreich, Ungarn und Deutschland konzentriert sich auf die sogenannten Mikrogliazellen im Gehirn. Diese sind Teil des Immunsystems des Gehirns und fungieren dort gewissermaßen als Reinigungsdienst. Die Studie zeigt, dass sich die Mikrogliazellen über so genannte Nanotunnel mit den Nervenzellen verbinden können. Sie nutzen diese Verbindung, um toxische Proteine, die sich in den Neuronen ansammeln können, abzusaugen und sichern so das Überleben der Nervenzelle.
Unsere Ergebnisse legen nahe, dass dieser Mechanismus eine entscheidende Rolle bei der Bekämpfung der Neurodegeneration spielt. Der nächste Schritt wäre jetzt, Medikamente zu entwickeln, die die Mikroglia stärken, Entzündungen begrenzen und so positive Effekte stärken.
Eine andere Forschungsrichtung zielt auf die Untersuchung von Umwelteinflüssen wie der Luftverschmutzung. Eine unserer neuen Studien auf Basis von Daten aus den Niederlanden zeigt, dass Luftverschmutzung schon bei einer relativ niedrigen Belastung das Alzheimer-Risiko erhöht. Das ist besorgniserregend.
Inwieweit kommt Luxemburgs Forschung den Patienten hier im Land zugute?
Mit unserer Forschung machen wir darauf aufmerksam, wie wichtig es ist, sich um die Patienten mit neurodegenerativen Krankheiten zu sorgen. Wichtig ist eine Diagnose, die andere, behandelbare Gedächtnisstörungen ausschließt. Die Patienten sollten auch Zugang erhalten zu allen Therapien, die heute schon möglich sind. Die Medikamente sollten vom Neurologen verschrieben werden, und die Patienten sollten von einer erfahrenen, auf Demenzerkrankungen spezialisierten Gedächtnisambulanz betreut werden. Wir versuchen derzeit, gemeinsam mit den Klinikern eine solche Forschungsambulanz einzurichten.
Manchen Patienten hilft es auch, an Studien teilzunehmen und sich so weniger ausgeliefert zu fühlen. Und generell steigt durch unsere wissenschaftlichen Aktivitäten und Publikationen natürlich im Ausland das Interesse an unserer Forschung hier in Luxemburg. Das wird letztlich allen Patienten zugute kommen.
Und welchen Stellenwert hat Luxemburgs Alzheimer-Forschung aus internationaler Sicht?
Qualitativ sind einzelne Forschergruppen aus Luxemburg auf Augenhöhe mit Forschern weltweit. Aber Luxemburg ist klein und die Forschungsinstitute hier verfügen nur über einen Bruchteil der Forschungsmittel und Mitarbeiterzahlen im Vergleich zu den großen Forschungsinstitutionen in der Welt, mit denen wir im wissenschaftlichen Wettstreit liegen. Zudem ist neurobiologische Forschung teuer, und die Lohnkosten in Luxemburg sind hoch. Wichtig ist deshalb, klare Schwerpunkte zu setzen. Deshalb konzentrieren wir uns am LCSB vor allem auf die Erforschung von Parkinson und Alzheimer. Außerdem wollen wir die Zusammenarbeit unserer verschiedenen Disziplinen wie der Bioinformatik und translationaler Forschung weiter stärken und so Synergien nutzen. Wir müssen in Luxemburg über lange Zeit einfach härter arbeiten als die wissenschaftliche Konkurrenz. Zielstrebigkeit ist ein Faktor, den man nicht unterschätzen sollte.
Autorin: Britta Schlüter
Redaktion: Jean-Paul Bertemes (FNR)
Infobox
Die „Association Luxembourg Alzheimer“ (ala) ist ein auf die Betreuung demenzkranker Menschen spezialisiertes Hilfs- und Pflegenetz. Seit ihrer Gründung im Jahr 1987 setzt sich die Vereinigung national und international für die Belange von Menschen mit Demenzerkrankungen und für deren Familien ein. Ala unterhält Beratungsdienste wie zum Beispiel psychologische und therapeutische Dienste, Selbsthilfegruppen, Tagesstätten sowie ein Wohn- und Pflegeheim.
Kontakt: https://ala.lu/de/
Helpline: Tel. 26 432 432