Divya Balakrishnan
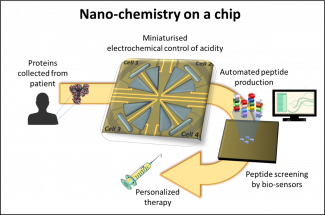
Représentation schématique du développement d'une thérapie personnalisée à l'aide de la nanochimie sur une puce.
Ces dernières années, nous avons assisté à une accélération des progrès de la médecine personnalisée. L'objectif final est de proposer à chaque patient un traitement adapté aux caractéristiques individuelles de son organisme et de sa maladie. Des éléments de la médecine personnalisée jouent déjà un rôle dans le traitement des patients atteints d’un cancer et transforment les résultats cliniques de certains d'entre eux. Cependant, le développement de traitements personnalisés est ralenti par plusieurs défis technologiques.
L'un de ces défis est la capacité de cribler un grand nombre de molécules thérapeutiques afin d'identifier le candidat idéal pour un traitement du cancer. Divya Balakrishnan et ses collègues du Luxembourg Institute of Science and Technology (LIST) ont mis au point un dispositif électrochimique à l'échelle nanométrique qui pourrait faciliter ce processus. Le dispositif contrôle automatiquement l'acidité dans les microréacteurs (en très petits volumes sur une puce), ce qui permet aux scientifiques de fabriquer et de cribler rapidement un grand nombre de candidats thérapeutiques à petite échelle. Il pourrait s’agir d’une solution à l'un des obstacles à la mise au point de thérapies personnalisées abordables pour les patients atteints d’un cancer.
Les travaux de Divya sont décrits dans sa thèse de doctorat intitulée « Acidity control in miniaturized volumes: engineered microreactors for high throughput chemical reactions », qui a été retenue dans la sélection finale du FNR Award 2020 dans la catégorie « Thèse de doctorat exceptionnelle ». (https://research.utwente.nl/en/publications/acidity-control-in-miniaturized-volumes-engineered-microreactors-)
Comment mettre au point une thérapie personnalisée contre le cancer en utilisant la nanochimie sur une puce?
Un vaccin thérapeutique contre le cancer est un type de thérapie contre le cancer qui pourrait être développé à l’aide de la nanochimie sur une puce. Différent d'un vaccin prophylactique qui protège un individu contre une maladie infectieuse, ce traitement pourrait inciter le système immunitaire du patient à attaquer et éliminer les cellules cancéreuses. Étant donné que les cellules cancéreuses sont des versions mutées de nos cellules saines, elles peuvent fabriquer d'autres protéines que les cellules saines. Les protéines sont de grandes molécules complexes qui ont de nombreuses fonctions essentielles dans notre organisme et sont constituées d'unités plus petites appelées peptides. L'analyse de ces peptides dans les cellules cancéreuses de chaque patient pourrait aider les médecins à sélectionner les meilleurs candidats pour un vaccin thérapeutique.
Les méthodes actuellement utilisées pour choisir les peptides qui pourraient avoir un effet thérapeutique sont laborieuses, coûteuses et peu efficaces. La technologie inventée par Divya rend ce processus plus rapide, plus fiable et moins coûteux, car il peut être mis en œuvre à un débit élevé et à petite échelle. À l'aide du dispositif électrochimique qui adapte automatiquement l'acidité, les peptides sont fabriqués à partir de la matière protéique isolée du patient. Les peptides sont criblés par un biocapteur qui sélectionne les meilleurs candidats pour un vaccin, qui peut ensuite servir de traitement pour les patients.
Pourquoi est-il important de contrôler l'acidité lors de la fabrication de molécules ?
La fabrication de molécules, telles que l'ADN, les protéines ou les peptides, se fait à une acidité (pH) spécifique. Plus les adaptations de l'acidité sont rapides et précises, plus la fabrication des molécules est efficace. C'est pourquoi le contrôle de l'acidité est essentiel en chimie combinatoire, qui consiste à fabriquer rapidement un grand nombre de composés chimiques à petite échelle et en un seul processus. Dans une expérience simple, l'acidité peut être contrôlée dans un verre d'eau en ajoutant alternativement des gouttes d'acide (par exemple du jus de citron ou du vinaigre) pour diminuer le pH et des gouttes de base (par exemple du chlore) pour l’augmenter. Étant donné que la génération d'une molécule compte plusieurs étapes et que chacune d’entre elles peut nécessiter un pH différent, l'adaptation de l'acidité lors de la fabrication de molécules à grande échelle devient laborieuse. Elle devient aussi de plus en plus difficile dans les petits volumes réactionnels. C'est précisément ce qui rend la technologie du contrôle automatisé de l'acidité dans les microréacteurs (dont la taille est inférieure à un demi-millimètre) si novatrice. Comme Divya l’explique : « Nous avons prouvé que plusieurs de ces microréacteurs peuvent travailler simultanément sur une puce d’une taille inférieure à une pièce de cinq centimes pour offrir la plus grande plage d'acidité des dispositifs électrochimiques actuellement disponibles. »
Quelles sont les utilisations futures possibles du contrôle automatisé de l'acidité ?
Divya Balakrishnan fait désormais partie d'une équipe de spécialistes en sciences des matériaux, de chimistes, d'immunologistes et d'informaticiens qui collaborent avec des collègues d'autres instituts de recherche européens dans le cadre d'un réseau bénéficiant d'un soutien de l'UE appelé Electromed. L'objectif de cette vaste collaboration est de développer une technologie de nouvelle génération qui ferait progresser la médecine personnalisée. Comme Divya l’a expliqué : « Selon un article sur la biopharmacie, au cours des dix dernières années, les coûts de mise au point d'un nouveau médicament s’élevaient à environ 1 milliard de dollars, les coûts les plus élevés étant associés aux médicaments contre le cancer et ceux utilisés en immunologie. La chimie combinatoire a été introduite il y a près de 30 ans. Il ne fait aucun doute qu’il faut trouver de nouvelles solutions innovantes capables de répondre aux demandes actuelles. Je suis convaincue que l'une d'entre elles sera notre nanochimie sur une puce, qui offre des traitements personnalisés fiables, peu coûteux et rapides développés ici au Luxembourg. »
L'atout supplémentaire de cette technologie est que, si elle s'avère aussi efficace et fiable que les chercheurs l’escomptent, elle pourrait aussi devenir intéressante dans d’autres domaines, tels que l'industrie alimentaire et les études environnementales.
Auteur : Anna Keller
Editeur : Michèle Weber (FNR)
Illustration: Divya Balakrishnan (LIST)