AdobeStock/nobeastsofierce
Illustration de bactéries en forme de bâtonnet. Des mutations génétiques des bactéries (indiquées ici par un changement de couleur) peuvent entraîner une résistance aux antibiotiques.
La résistance aux antibiotiques menace la santé mondiale et « nécessite que des mesures soient prises d’urgence », selon l’OMS. Pour l’Union européenne, il s’agit de l’une des trois menaces sanitaires prioritaires. Un moyen d’action central est de réduire leur consommation, autant en médecine humaine que vétérinaire. Les efforts ont-ils porté, et ont-ils fait baisser les résistances ? De nouvelles molécules pour traiter des bactéries résistantes pourraient-elles être bientôt à disposition?
Nous résumons ici ce que la science nous dit de la consommation des antibiotiques au Luxembourg et dans le monde, de l’évolution des résistances, et des perspectives de nouveaux moyens de lutte contre les bactéries. Ce fact check aborde les questions suivantes :
- Que sont les antibiotiques et comment fonctionnent-ils ?
- Pourquoi y a-t-il des bactéries résistantes aux antibiotiques ?
- Quels sont les dommages provoqués par les résistances ?
- Comment lutter contre les résistances aux antibiotiques ?
- Avons-nous baissé la consommation d’antibiotiques ?
- Les résistances ont-elles baissé ?
- Peut-on espérer de nouveaux antibiotiques ?
Dr. Jacques Zimmer, chercheur au Luxembourg Institute of Health et des membres du groupe de travail « Surveillance » du Plan National Antibiotiques au Luxembourg ont donné leur conseils lors de la rédaction de cet article.
Résumé
Les antibiotiques constituent un pilier de la médecine moderne, mais leur efficacité est de moins en moins garantie. La raison est l’augmentation de bactéries résistantes aux antibiotiques et à la diffusion de germes multirésistants dans l’environnement et la population.
Si le développement de bactéries résistantes est un phénomène naturel et inévitable, il se voit accéléré par une utilisation plus fréquente et élargie des antibiotiques. Une utilisation plus élargie d'antibiotiques est bénéfique lorsque les antibiotiques sont utilisés pour soigner des maladies infectieuses – parfois fatales si non traitées – et améliorent ainsi la santé des populations, notamment dans les pays à faible revenu. Mais une partie importante des antibiotiques sont consommés sans bénéfices médicaux. C’est notamment le cas lors de prescriptions injustifiées, d’utilisations incorrectes par les patients, ou d’un emploi inapproprié dans l’élevage. Cette surconsommation favorise le développement de bactéries résistantes aux antibiotiques. Il est crucial de ralentir ce dernier afin d’éviter des impasses thérapeutiques d’ici quelques années.
Des progressions rapides des résistances aux antibiotiques ont été observées depuis la fin des années 1990. Elles semblent se stabiliser en partie dans l’UE au cours des dernières 20 années, et au Luxembourg il y a des premiers signes – sur base de données encore très limitées – qui montrent dans la même direction au cours des dernières années. Le Luxembourg a baissé la consommation d’antibiotiques depuis dix ans: d’un quart dans la santé humaine et presque de moitié dans l’élevage. Mais la proportion de bactéries résistantes reste très élevée et l’OMS rapporte des niveaux « alarmants » au niveau mondial.
Les milieux de la santé aimeraient disposer de nouvelles substances ne connaissant pas (encore) de résistances, mais la découverte et la commercialisation des produits novateurs ont fortement ralenti depuis un demi-siècle. Une raison se trouve dans le manque d’incitations économiques pour les entreprises pharmaceutiques à investir dans ce marché peu rentable. Des nouvelles approches comme l’immunothérapie ou l'utilisation de virus destructeurs de bactéries sont également en développement. Les vaccins constituent également un moyen de prévention important contre les infections bactériennes.
Nous avons également résumé l'état des lieux scientifique de ce sujet dans une courte vidéo « Ziel mir keng! » qui a été publiée sur la chaîne YouTube de science.lu après diffusion sur RTL Télé Lëtzebuerg dimanche soir, 24 novembre 2024 dans le cadre de l'émission PISA - de Wëssensmagasin.
Que sont les antibiotiques et comment fonctionnent-ils ?
Les antibiotiques sont des substances qui tuent les bactéries ou empêchent leur croissance. On les utilise dans la médecine humaine pour traiter des infections bactériennes à l’origine de nombreuses maladies telles que des pneumonies, sinusites, otites, infections urinaires, méningites ainsi que des maladies moins fréquentes dans nos régions comme la syphilis, la tuberculose, la lèpre, la diphtérie, le typhus, le choléra et le tétanos. L’impact des antibiotiques est massif: la mortalité due aux maladies infectieuses a chuté de 70 % aux Etats-Unis et en Angleterre depuis l’introduction de la pénicilline en 1942.
Ils sont également employés de manière prophylactique afin d’éviter l’apparition d’une infection dans des situations de risque, comme lors d’interventions chirurgicales (dont les transplantations, les césariennes et certaines interventions orthopédiques), lorsqu’une personne a un système immunitaire affaibli (par exemple lors d’une chimiothérapie contre un cancer, etc.) ou encore lors de certaines infections chroniques.
Malgré le succès des antibiotiques, les infections bactériennes représentent encore un risque sanitaire majeur. On estime qu’elles sont associées à environ un décès sur sept autour du monde, soit 13,7 millions en 2019. La moitié sont dues à seulement cinq bactéries: Staphylococcus aureus, Escherichia coli, Streptococcus pneumoniae, Klebsiella pneumoniae et Pseudomonas aeruginosa. Elles peuvent notamment provoquer des infections des voies respiratoires (comme la pneumonie), du sang (la septicémie), du système nerveux central (par exemple des méningites) ou encore de l’appareil digestif.
Des antibiotiques sont aussi utilisés dans la médecine vétérinaire pour traiter des infections bactériennes, et également de manière prophylactique dans certains cas décrits plus bas.
Les antibiotiques peuvent être d’origine naturelle (ils sont secrétés par des bactéries, des champignons ou encore des éponges), être purement synthétiques ou, être issus de modifications de composés naturels.
Les antibiotiques peuvent avoir des effets secondaires à court terme (nausée, diarrhée et réactions allergiques) ainsi qu’à long terme, lorsqu’ils déséquilibrent la flore intestinale et favorisent des maladies de l’appareil digestif. L’autre inconvénient est que leur utilisation favorise l’apparition de bactéries résistantes (voir reste de l’article).
Comment les antibiotiques fonctionnent
L’OMS dénombre 258 antibiotiques. Le premier antibiotique était le Salvarsan, commercialisé en 1911 contre la syphilis. La célèbre pénicilline fut découverte par Fleming en 1928 mais a dû attendre 1942 avant d’être employée pour soigner des malades.
Les antibiotiques agissent de plusieurs manières. Certains tuent les bactéries en empêchant le maintien de leur enveloppe externe (par exemple les polymyxines ainsi que les bêtalactamines telles que les pénicillines et céphalosporines) ou en bloquant la réplication de l’ADN bactérien (p. ex. les quinolones). D’autres ralentissent ou stoppent la croissance des bactéries en agissant sur le métabolisme bactérien (p. ex. les sulfamides) ou en inhibant la synthèse des protéines (p. ex. les tétracyclines, les macrolides, et autres).
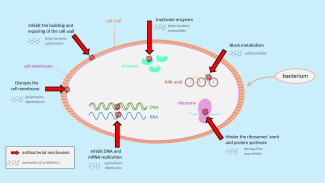
Illustration 1. Les différentes classes d’antibiotiques agissent de manière variée sur les bactéries. Certaines s’attaquent à leur enveloppe, d’autres perturbent leur métabolisme ou la synthèse des protéines.
Infobox
Les désinfectants et les antiseptiques – tels que l’alcool, l’eau oxygénée, les dérivées du chlore (eau de Javel) ou d’iode (Bétadine) – sont moins spécifiques que les antibiotiques et agissent le plus souvent également contre d’autres types de microbes (virus et champignons). On applique les désinfectants sur des surfaces inertes (tables, instruments, etc.) et les antiseptiques sur le corps (sur la peau, les muqueuses ou les plaies). Les antibiotiques, eux, sont administrés par voie orale (pilule), par injection (intraveineuse ou dans un muscle), ou par voie locale (crème ou liquide pour la peau, les yeux, les oreilles, etc.). Les désinfectants ou antiseptiques sont donc appliqués localement sur des surfaces limitées tandis que les antibiotiques sont souvent administrés de manière systémique, à savoir dans le corps entier.
Les antiseptiques et désinfectants agissent par exemple en dégradant la membrane des bactéries (alcool, iode) ou comme des agents oxydants qui perturbent le rôle joué par les protéines dans les microbes (eau de Javel, eau oxygénée).
Pourquoi y a-t-il des bactéries résistantes aux antibiotiques ?
Les bactéries développent de manière naturelle des résistances aux substances utilisées contre elles, à l’instar des autres microbes. Il s’agit d’un phénomène inévitable lié à la sélection naturelle et auquel nous devons nous adapter. Certaines souches de bactéries possèdent donc – de manière innée ou suite à des mutations – des spécificités qui les protègent contre un antibiotique, et vont ainsi survivre en plus grand nombre que les autres souches. Leur population croît davantage, ce qui augmente la proportion générale de bactéries résistantes existantes dans l’environnement.
La résistance se transmet naturellement aux descendants, mais peut également se propager par un transfert de gènes lorsqu’une bactérie absorbe de l’ADN d’une autre. La résistance peut alors se répandre rapidement dans d’autres souches bactériennes.
Certaines bactéries ont développé des résistances à plusieurs antibiotiques depuis les années 1970-1980. Ces bactéries multirésistantes se sont diversifiées et ont diffusé dans l’environnement après 1990. Des bactéries hautement résistantes ont été observées dans les années 2000 avant de se répandre à partir de 2010.
Vidéo en haut: Cette expérience filmée par des scientifiques du laboratoire de Kishony de la Harvard Medical School et de Technion (www.technion.ac.il/en/) montre de manière impressionnante les mouvements de bactéries lorsqu'elles sont confrontées à des doses de plus en plus élevées d'antibiotiques et qu'elles s'adaptent pour y survivre et s'y développer. Source.
Mauvaises utilisations des antibiotiques
L’émergence de résistances est un phénomène inévitable, mais elle s’est accélérée en raison du contact plus fréquent des bactéries avec des antibiotiques. L’augmentation générale de l’usage des antibiotiques en médecine humaine en est une première raison, une étude estimant que la consommation d’antibiotique par personne dans le monde a augmenté de 46 % en moins de vingt ans entre 2000 et 2018.
Un problème central dans ce domaine réside dans l’usage inapproprié des antibiotiques. Ils sont souvent prescrits sans indication justifiée ou mal utilisés, ce qui accélère l’essor des résistances sans apporter un bénéfice sanitaire clair. Environ 20 à 30 % des antibiotiques seraient ainsi prescrits de manière inutile, par exemple pour traiter la grippe ou un rhume dû à un virus et non pas à une bactérie. Les antibiotiques sont également souvent mal utilisés, lorsque les doses et durées de traitement ne sont pas respectées. Cela réduit les chances que le traitement éradique les bactéries visées, laissant alors des survivantes s’échapper et propager des résistances.
Un problème de taille reste également l’emploi d’antibiotiques dans l’élevage d’animaux de rente. Dans certains pays, il est encore effectué à large échelle et de manière préventive, ainsi que comme facteur de croissance afin d’accélérer la prise de poids des animaux (une pratique interdite dans l’UE depuis 2006). Par exemple, la majorité (entre deux tiers à trois quarts) des ventes d’antibiotiques aux Etats-Unis est destinée à l’élevage, le reste à la médecine humaine.
L’utilisation d’antibiotiques comme facteurs de croissance dans l’alimentation animale est interdite dans l’UE depuis 2006. L’importation de produits animaux ou d’animaux ayant reçu des aliments médicamenteux n’est plus autorisée depuis 2022. Toutefois, l’utilisation d’antibiotiques en cas de maladie ou à des fins prophylactiques est permise pour autant qu’elle soit encadrée et non systématique.
Tous ces antibiotiques viennent en contact avec les très nombreuses bactéries (nocives ou inoffensives) qui résident dans l’environnement, dans les animaux et dans notre corps. Ceci accélère le développement de souches possédant des résistances et la transmission de ces dernières.
Quels sont les dommages provoqués par les résistances ?
La proportion importante de bactéries résistantes à un ou même à plusieurs antibiotiques pose des problèmes sanitaires et économiques significatifs. Une maladie infectieuse traitée avec un antibiotique inefficace va s’aggraver et générer des risques sanitaires: durée de maladie et traitement plus longue, prolongation de l’hospitalisation, complications. Elle pourra avoir une issue fatale, notamment en présence d’une bactérie résistante à tous les antibiotiques disponibles sur le marché.
Dans le cas d’une utilisation prophylactique, par exemple lors d’une intervention chirurgicale ou d’une chimiothérapie, un antibiotique inefficace ne sera plus en mesure de prévenir des infections. Celles-ci exposeront les patients à des complications et pourront prolonger leur hospitalisation et mettre leur santé en danger. L’essor des résistances rend plus fréquentes et plus dangereuses les infections nosocomiales, qui surviennent lors d’un séjour à l’hôpital. Elles sont liées à la concentration de personnes malades infectés, à l’immunité affaiblie des patients ainsi qu’aux gestes de soins.
Les bactéries résistantes aux antibiotiques ont provoqué la mort d’environ 35 000 personnes dans l’EU/EEA en 2020. Une large étude estimait 1,27 million de morts autour du monde en 2019 (soit le double des décès provoqués par des maladies telles que le paludisme ou que le SIDA). Elle estimait à quatre fois plus grand le nombre de décès non pas seulement attribués mais également associés aux bactéries résistantes (4,95 millions), à savoir des cas où il n’est pas clair si l’infection était l’unique raison du décès. La même équipe de recherche estimait à 7,7 millions le nombre de décès associés aux bactéries en général, qu’elles soient résistantes ou non, indiquant que les souches résistantes sont associées à deux tiers des décès liés aux bactéries.
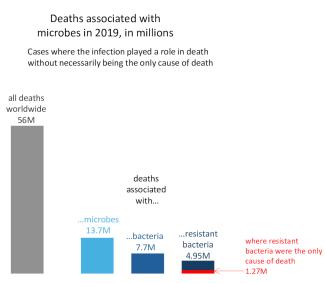
Illustration 2 : Une étude estime que les bactéries résistantes étaient la cause unique de 1,27 million de décès autour du monde en 2019. Près de 5 millions de décès ont été associés à des bactéries résistantes sans que ces infections en aient été forcément l’unique cause – soit deux tiers des 7,7 millions de morts associées à des infections avec des bactéries résistantes ou non. Environ 6 millions sont associés à d’autres infections microbiennes (virus, champignons, parasites), sur un total de 56 millions de morts en 2019. (Source)
Une mise à jour publiée en septembre 2024 analyse l’évolution sur les trente dernières années et constate que les tendances varient de manière substantielle selon l’âge et le lieu. Les décès attribués aux bactéries résistantes ont diminué de plus de moitié chez les enfants de moins de 5 ans, mais ont augmenté de 80 % pour les adultes de 70 ans et plus. Selon des projections pour 2050, 1,9 million de décès pourraient être attribués (et 8,2 millions associés) aux bactéries résistantes au niveau mondial.
Comment lutter contre les résistances aux antibiotiques?
Moins et mieux consommer, et surveiller
Pour lutter contre les bactéries résistantes, il est crucial de réduire les quantités d’antibiotiques utilisées en médecine et dans l’élevage. Il est également important de cibler les traitements – en s’assurant par exemple qu’une infection est bactérienne et non pas virale et en choisissant un antibiotique ciblant les bactéries responsables sur base d’un diagnostic microbiologique. Il faut également prescrire le moins possible les molécules rencontrant actuellement encore peu de résistances : le but est alors de les garder en réserve en tant que thérapies « de dernier recours » qui ne doivent être employées que lorsque les antibiotiques standards ne sont plus efficaces et sur avis de médecins infectiologues.
Un autre axe important est de surveiller la consommation des antibiotiques, les germes multirésistants et l’évolution des résistances. Il faut également étudier les voies de transmission des résistances: entre bactéries, du sol aux plantes, des animaux aux humains, chez les vétérinaires ou encore via les gens rentrant de voyage. L’objectif est d’anticiper la prolifération des résistances et de déterminer des moyens d’intervention.
Plusieurs organisations, dont l’OMS, ont lancé depuis des dizaines d’années des appels à réagir devant l’essor des résistances. Elles promeuvent l’approche dite « Une seule santé » (« One Health » qui englobe les interactions entre les humains, les animaux et l’environnement. Depuis les années 2000, de nombreux Etats – dont le Luxembourg en 2018 – ont lancé des programmes nationaux visant à réduire la consommation d’antibiotiques et à surveiller la situation.
Avons-nous baissé la consommation d’antibiotiques?
En médecine humaine
Au Luxembourg
La consommation d’antibiotiques au Luxembourg en médecine humaine a baissé d’un quart entre 2012 et 2022. Cette réduction s’observe pour les antibiotiques délivrés en pharmacie ainsi que pour ceux administrés en milieu hospitalier, ces derniers représentant environ 7 % du total.
Un rebond fut observé en 2022 au Luxembourg ainsi que dans d’autres pays européens. Il suit la baisse abrupte observée durant la première phase de la pandémie de Covid-19 et liée à des infections moins fréquentes en raison des mesures sanitaires mises en place (masques, désinfection, confinement, consultations médicales moins fréquentes). Les comparaisons doivent être faites avec prudence, le processus de traitement des données ayant changé au Luxembourg en 2020.
Infobox
Les quantités d’antibiotiques consommées ou prescrites au niveau national sont généralement exprimées en nombre de doses définies journalières (DDJ) par mille habitants et par jour, la DDJ étant la dose recommandée de l’antibiotique lors d’un traitement standard. Par exemple, la consommation des pénicillines au Luxembourg d’environ 8 DDJ/1000 habitants/jour en 2022 indique que 8 personnes sur 1000 en moyenne prenaient chaque jour la dose standard. A noter que ces doses varient suivant les antibiotiques et les infections.
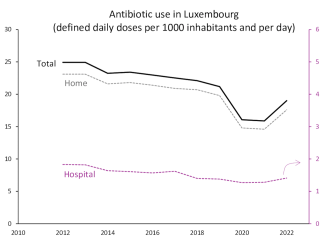
Illustration 3 : Consommation d’antibiotiques au Luxembourg en milieu hospitalier (axe de droite) et communautaire (axe de gauche), en nombre de doses journalières usuelles par mille habitants. (Source)
Le Luxembourg a adopté en 2018 un plan national afin de lutter contre l’émergence des résistances et contre leur transmission. Il suit l’approche « Une seule santé », qui aborde la santé humaine en incluant les questions de santé animale et environnementale. Il s’agit en particulier de surveiller la consommation d'antibiotiques et la propagation des résistances aux antibiotiques en santé humaine et animale ainsi que d’analyser les résidus dans les denrées alimentaires. Ceci dit, des initiatives pour réduire la consommation d’antibiotiques chez les humains ont déjà été lancées depuis plus de vingt ans au Luxembourg, par exemple au moyen de campagnes d’information grand public.
En Europe
L’utilisation d’antibiotiques est fortement contrastée dans l’Union européenne, avec une consommation quatre fois plus grande à Chypre ou en Grèce qu’aux Pays-Bas. Les pays consommant le moins d’antibiotique se trouvent principalement au Nord et en Europe centrale, les gros consommateurs étant plutôt au Sud et à l’Est du continent.
Le Luxembourg se trouve en 2022 au 16e rang sur 29 pays avec une valeur de 19,1 doses définies journalières par mille habitants par jour, juste en dessous de la moyenne de l’UE (19,4). La plupart des pays ont stabilisé ou réduit leur consommation, mais certains la voient augmenter, comme la Lettonie, le Portugal ou l’Irlande.
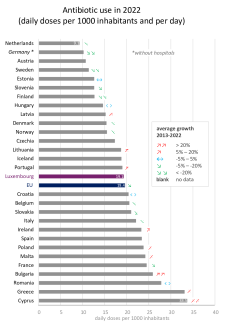
Illustration 4 : Consommation d’antibiotiques dans l’UE en 2022, en dose journalière par 1000 habitants et par jour (milieu communautaire et hospitalier). Les flèches indiquent une baisse forte (↘↘) ou modérée (↘), l’absence d’évolution marquée (↔), et une croissance modérée (↗) ou forte (↗↗). L’évolution n’est pas donnée pour tous les pays, notamment pour le Luxembourg en raison d’un changement de méthode en 2020. (Source)
Dans le monde
La consommation d’antibiotique par personne dans le monde a augmenté de 46 % en moins de vingt ans entre 2000 et 2018. Cette croissance s’observe principalement dans les régions à faible revenu, une évolution bienvenue liée à un accès croissant à ces médicaments essentiels.
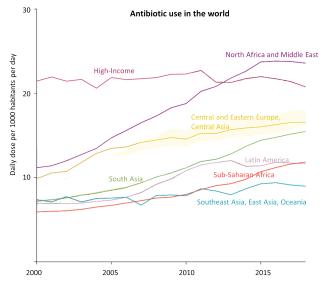
Illustration 5 : La consommation d’antibiotique a augmenté partout dans le monde depuis 2000 à l’exception des pays à hauts revenus, où elle est restée stable. Elle a plus que doublé en 18 ans en Afrique du Nord/Moyen-Orient ainsi qu’en Asie du Sud. (Source)
Les antibiotiques de derniers recours
Freiner l’essor des résistances exige d’utiliser les antibiotiques avec parcimonie, en particulier ceux qui sont encore très efficaces parce que récemment mis sur le marché. L’OMS a établi en 2017 une classification des antibiotiques en trois groupes:
- La catégorie « Access » rassemble les molécules devant être utilisée en premier et deuxième choix et dont la disponibilité doit être garantie. Elles sont ciblées et connaissent en général peu de résistances. Exemples: ampicilline, doxycycline, métronidazole.
- La catégorie « Watch » regroupe les antibiotiques à large spectre (pouvant lutter contre de nombreux types de bactéries) ayant le potentiel de traiter des bactéries résistantes. Ils ne devraient être utilisés que lorsque les médicaments du premier groupe ne sont pas appropriés et sur base de résultats d’un diagnostic microbiologique. Exemples: ciprofloxacine, acide fusidique.
- La catégorie « Reserve » concerne des thérapies de dernier recours, à n’utiliser que dans les cas graves et uniquement si les autres traitements sont inefficaces, par exemple lorsqu’une infection est due à des bactéries résistant à plusieurs types d’antibiotiques, dites multirésistantes. Exemple: daptomycine.
L’OMS recommandait en 2023 d’utiliser au moins 60 % d’antibiotiques de la catégorie Access afin de préserver au mieux les deux autres catégories. Cette catégorie représente au Luxembourg 60,8 % des produits délivrés en 2022, en respect avec cette recommandation. Cette valeur n’atteint par contre pas encore l’objectif de 65 % énoncé par le Conseil de l’UE pour 2030.
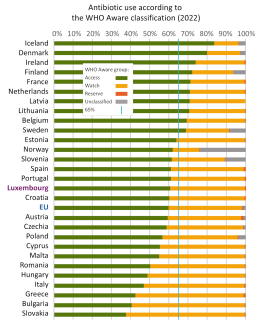
Illustration 6 : Proportion des antibiotiques consommés dans l’EU selon les trois catégories de l’OMS Aware. La première catégorie, Access, devrait être au moins 65 % d’ici 2030 selon les recommandations du Conseil de l’UE. (Source)
Moins d’antibiotiques en médecine vétérinaire au Luxembourg
L’utilisation d’antibiotiques dans l’élevage d’animaux de rente a fortement baissé au Luxembourg, avec une concentration presque divisée par deux en dix ans (de 43 mg par kilo d’animal en 2012 à 25 mg/kg en 2022). La baisse réelle est probablement légèrement moins marquée, les statistiques ne tenant pas compte des antibiotiques achetés à l’étranger par les vétérinaires frontaliers et dispensé au Luxembourg (ces chiffres seront inclus dans un prochain rapport). A ces chiffres se rajoutent les antibiotiques utilisés pour les animaux de compagnie, environ 9% du total.
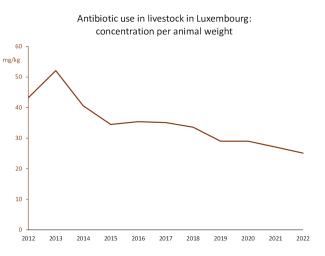
Illustration 7 : Le Luxembourg a fortement réduit l’usage d’antibiotiques dans l’élevage animaux producteurs de denrées alimentaires, divisant presque par deux leur concentration par kilo d’animal. (Source)
Le Luxembourg est l’un des pays de l’UE utilisant le moins souvent d’antibiotiques dans l’élevage: la concentration y est un tiers de moins qu’en France et presque trois fois moins qu’en Allemagne ou en Belgique. Les différences sont extrêmes, les valeurs allant de 2 mg/kg en Norvège à cent fois plus à Chypre avec 254 mg/kg.
En moyenne, l'utilisation d’antibiotiques en médecine vétérinaire a diminuée de 53 % entre 2011 et 2023 dans l’UE. Au niveau mondial, de nombreux pays ont également réussi ou sont en route de réduire leur utilisation d'antibiotiques dans l'agriculture dans des proportions similaires. Les États-Unis sont légèrement à la traîne, ayant réduit leur utilisation d'antibiotiques médicalement importants chez les animaux de rente de 33 % entre 2012 et 2021.
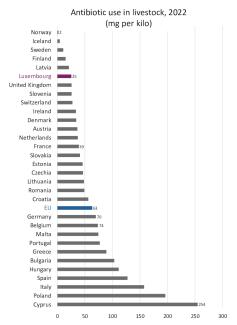
Illustration 8 : Le Luxembourg est l’un des pays de l’UE utilisant le moins souvent des antibiotiques dans l’élevage. (Source)
Les résistances ont-elles baissé?
Les appels à réduire et améliorer l’usage des antibiotiques ont été entendus et en partie appliqués, contribuant à freiner et stabiliser en partie l’essor des résistances.
Au Luxembourg
Les données disponibles sont encore très limités et donc on ne peut pas encore tirer des conclusion globales, mais uniquement parler d’indices ou premières tendances.
En médecine humaine, il y a des premiers indices que les résistances associées à des infections invasives (voir infobox) sont restées stables au Luxembourg ou ont baissé entre 2018 et 2022, mais avec certaines exceptions. Cette analyse concerne dix pathogènes suivis dans tous les pays de l’UE au sein de deux initiatives européennes. Ce monitoring évalue pour chaque pathogènes (E. coli, S. pneumoniae, E. faecalis, etc.) la proportion de bactéries résistantes à différentes classes d’antibiotiques (aminopénicillines, céphalosporines, carbapénèmes, etc.), voire à leur combinaison. Un exemple connu d’une telle bactérie multirésistante est le staphylocoque doré résistant à la méticilline (MRSA en anglais).
Infobox
Les données nationales sur les résistances bactériennes présentées dans le premier rapport de surveillance du Plan National Antibiotiques concernent les infections invasives touchant le sang ou le système nerveux. Elles sont transmises chaque année par les hôpitaux et les laboratoires privés au réseau European Antibiotic Resistance Surveillance (EARS-net). Un suivi national des résistances liées à des cas moins graves (infections urinaires, pulmonaires et autres) fait actuellement encore défaut, mais se fait dans les hôpitaux. Par contre, FWD-Net, le réseau de surveillance dédié aux agents pathogènes entériques (Salmonella, E. coli et Campylobacter) qui causent des maladies et zoonoses d'origine alimentaire et hydrique, surveille les données qui proviennent de tous les laboratoires de biologie clinique du Luxembourg.
On compte ainsi une quarantaine de paires pathogène-antibiotique. La plupart montrent des résistances stables ou en diminution. Par exemple, on trouvait en 2018 que 55% des souches de bactéries E. coli étaient résistantes aux ampicillines. Cette proportion est passée à 50% en 2022, mais reste à un niveau très élevé. Certaines paires montrent une augmentation des résistances, comme les salmonelles aux fluoroquinolones ou S. pneumoniae aux macrolides.
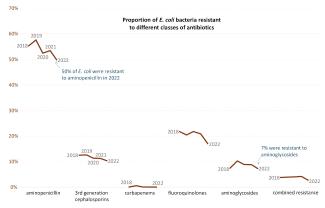
Illustration 9 : Evolution des résistances des bactéries E. coli à 5 antibiotiques et à leur combinaison. De tels graphiques existent pour les autres pathogènes suivis par le réseau européen EARS-Net. (Source)
En Europe
La situation est encore plus contrastée en Europe, des différences entre les pays se rajoutant aux paires bactérie-antibiotique. Une étude a analysé l’évolution de nombreuses paires pathogène-antibiotique dans des pays européens entre 1998 et 2019, et montre que l’augmentation des résistances n’est pas généralisée. Sur 887 triplets bactérie-anitbiotique-pays suivis, seuls 17% montraient des résistantes croissantes et la moitié était stable ou en voie de stabilisation.
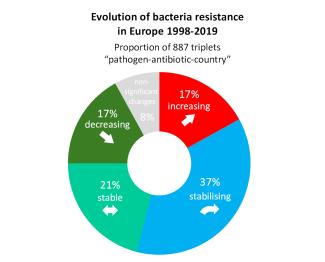
Illustration 10 : La plupart des paires pathogène-antibiotique comptées par pays européen présentent une résistance stable ou en voie de stabilisation. Un sixième diminue, alors qu’un autre sixième est en croissance. (Source)
Dans le monde
L’augmentation des résistances aux antibiotiques est un phénomène mondial et global, les microbes pouvant circuler entre les pays et propager ainsi les souches résistantes. L’OMS rapporte au niveau mondial des niveaux «alarmants» de résistance, avec des valeurs médianes sur 76 pays de 42% de souches bactériennes E. coli résistantes aux céphalosporines de troisième génération, de 35% de staphylocoques dorés résistants aux méticillines et de 20% pour les E. coli responsables d’infections urinaires contre les antibiotiques standards. Si l’OMS salue les progrès réalisés dans la surveillance des résistances au niveau mondial, elle souligne que les fortes disparités encore existantes rendent difficile l’analyse de la situation.
Peut-on espérer de nouveaux antibiotiques?
Peu de nouvelles substances
La découverte de nouveaux types d’antibiotiques a fortement ralenti: la dernière grande classe d’antibiotique a été découverte en 1987 (et mise sur le marché en 2003 seulement), contre 26 depuis les années 1920, selon l’initiative React (note: le nombre de types d’antibiotiques varie selon les diverses classifications). Un autre article mentionne 8 nouvelles classes d’antibiotiques mises sur le marché depuis les années 1980, contre 30 auparavant.

Illustration 11 : Les grandes classes d’antibiotiques ont été découvertes avant les années 1980. Depuis, les nouveaux composés sont rares. Certaines molécules ont pris plusieurs dizaines d’années avant d’être autorisées à être mis sur le marché. Entre-temps, des résistances à toutes ces classes d’antibiotiques ont été observées – parfois avant même leur commercialisation. (Source)
Les raisons de ce ralentissement sont diverses. Premièrement, les molécules les plus faciles à trouver ont déjà été identifiées, notamment durant l’âge d’or des antibiotiques entre 1940 à 1960. Deuxièmement, le marché motive peu les entreprises pharmaceutiques à investir dans la recherche de nouveaux composés. Elles préfèrent se tourner vers des marchés plus rentables tels que le cancer ou les problèmes respiratoires.
Une étude estime que développer un nouvel antibiotique coûte en moyenne 1,5 milliard de dollars et prend 12 ans. Contrairement à d’autres médicaments tels que les anticancéreux, les antibiotiques ne génèrent pas de revenus importants, vu leur utilisation limitée dans le temps. De plus, les nouvelles substances doivent souvent être consommées de manière très restreinte afin d’éviter le développement de résistance, étant gardées comme médicament de dernier recours, ce qui limite fortement leur vente. Un exemple a frappé les esprits: après avoir développé un nouvel antibiotique durant quinze ans, l’entreprise Achaogen le mit sur le marché en 2018 mais fit faillite un an après, n’ayant pu générer des ventes que pour un montant d’un million de dollars.
Des nouvelles thérapies
De nouveaux antibiotiques arrivent sur le marché, mais ne soulagent que peu le problème des résistances. Sur 23 molécules ou combinaisons de composés approuvées autour du monde entre 2013 et 2022, aucune d’entre elles n’agit à travers un mécanisme d’action nouveau – le dernier remontant à 2012. Douze nouveaux traitements ont été autorisés par les autorités américaines (FDA) ou de l’EU (EMA) entre 2017 et 2020, mais montrent peu d’avantages par rapport aux médicaments existants, et 80 % appartiennent à des classes d’antibiotiques qui connaissent déjà des résistances, selon l’OMS.
Quelque 217 nouvelles thérapies étaient en phase de développement précliniques (tests sur des cultures et sur des animaux) et 77 en phase clinique en 2021, selon l’OMS. Certains poursuivent des approches innovantes, notamment contre des pathogènes ayant développé des résistances multiples, mais l’OMS considère que les antibiotiques en phase clinique ou récemment approuvés sont «insuffisants pour relever le défi de l'émergence et de la propagation croissantes de la résistance».
La publication en 2024 de recherches introduisant une nouvelle classe d’antibiotique par l’entreprise suisse Roche a suscité des espoirs, tempérés cependant par des craintes liées au modèle économique actuel qui n’encourage que peu la commercialisation de nouveaux antibiotiques.
Les scientifiques développent d’autres approches pour lutter contre les bactéries, notamment des vaccins, l’immunothérapie ou encore l’utilisation de virus appelés «phages» détruisant les bactéries. Ces nouvelles méthodes fonctionnent de manière bien plus ciblée que les antibiotiques classiques, mais exigent de bien identifier les bactéries responsables de l’infection. Des résultats probants seront nécessaires avant de pouvoir les employer pour traiter les maladies infectieuses les plus fréquentes.
Infobox
Au Luxembourg Institute of Health (LIH), Jacques Zimmer et Carole Devaux travaillent sur de nouvelles stratégies pour combattre les bactéries résistantes. Ils développent des nouveaux composés qui activent le système immunitaire, une approche différente des antibiotiques traditionnels s’attaquant directement aux pathogènes. Ces composés comprennent des fragments d'anticorps qui ciblent les cellules tueuses naturelles de notre système immunitaire et les activent contre les bactéries. Une approche similaire est employée en oncologie pour traiter certains types de cancer.
Auteur : Daniel Saraga (Saraga Communications)
Illustrations : Daniel Saraga
Éditeur : Michèle Weber (FNR)
Conseils : Jacques Zimmer (LIH) et groupe de travail du Plan National Antibiotiques (Direction de la Santé)
Infobox
HERA factsheet - HEALTH UNION: Identifying top 3 priority health threats
It's time to fix the antibiotic market
Antimicrobial resistance: A frightening and complex public health challenge
Antiseptics and Disinfectants: Activity, Action, and Resistance
Global antibiotic consumption and usage in humans, 2000-18: a spatial modelling study
Research reveals levels of inappropriate prescriptions in England
Unnecessary Antibiotic Prescribing in US Ambulatory Care Settings, 2010–2015
Antibiotics shape microbiota and weight gain across the animal kingdom
Global Trends in Antimicrobial Use in Food Animals from 2017 to 2030
HealthforAnimals, 2024. How Prevention Can Reduce the Need for Antibiotics. Brussels
WOAH. 2023. Annual Report on Antimicrobial Agents Intended for Use in Animals, 7h Report
Surveillance of antimicrobial resistance in Europe, 2022 data
Global burden of bacterial antimicrobial resistance in 2019: a systematic analysis
WHO: Fact Sheet, Malaria [Consulted July 2024]
WHO: Number of people dying of HIV-related causes, 2023 [Consulted July 2024]
Plan National Antibiotiques (2018-2022)
Global antibiotic consumption and usage in humans, 2000–18: a spatial modelling study
Antimicrobial consumption in the EU/EEA (ESAC-Net), Annual Epidemiological Report 2022
Antibiotiques: pour qu’ils restent efficaces, n’en abusons pas!
Temporal Trends in Antibiotic Resistance in Europe, 1998-2019
Global geographic trends in antimicrobial resistance: the role of international travel
Antimicrobial resistance, WHO [Consulted August 2024]
Global antimicrobial resistance and use surveillance system (GLASS) report 2022, WHO
Few antibiotics under development
Antibiotics: past, present and future
Antibiotics in the clinical pipeline as of December 2022
2021 Antibacterial agents in clinical and preclinical development: an overview and analysis, WHO
A new class of antibiotics is cause for cautious celebration — but the economics must be fixed






