© LIH
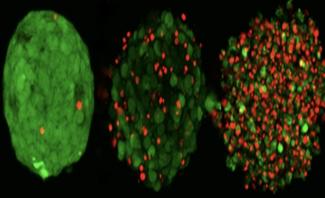
Die Veränderung der 3D-Organoide während der medikamentösen Behandlung: die gesunden Zellen sind grün, die abgestorbenen sind rot
Klinische Studien sind wichtig, um die Wirksamkeit neuartiger therapeutischer Arzneimittel direkt an Patienten zu testen. Ihr Erfolg hängt wesentlich von der Qualität der Ergebnisse ab, die in präklinischen Arzneimittelteststudien vor der klinischen Phase an experimentellen Modellen von Patiententumoren erzielt werden. Die Verfügbarkeit präziser und umfassender Modelle im präklinischen Bereich, die das gesamte Spektrum der bei Hirntumoren beobachteten genetischen Variationen widerspiegeln und die in der Lage sind, die Reaktion bestimmter Tumorarten auf neue personalisierte Behandlungen zuverlässig vorherzusagen, ist daher von größter Bedeutung.
Tumor-Organoide: 3D-Gewebekulturen aus Tumorzellen von Patienten
Um diesem derzeit ungedeckten Bedarf gerecht zu werden, hat das Neuro-Onkologie-Labor NORLUX der Abteilung für Onkologie des Luxembourg Institute of Health (LIH) eine Sammlung an Hirntumoren von über 1000 Patienten angelegt - in Zusammenarbeit mit dem Centre Hospitalier de Luxembourg (CHL), dem Laboratoire National de Santé (LNS), dem Luxembourg Centre for Systems Biomedicine (LCSB) der Universität Luxemburg und anderen internationalen Partnern. Mit Hilfe der von der neurochirurgischen Abteilung des CHL zur Verfügung gestellten Proben konnte NORLUX eine Biobank von Hirntumor-Organoiden erstellen.
Es handelt sich bei diesen Organoiden um dreidimensionale Gewebekulturen, die aus lebensfähigen Zellen von Patiententumoren gewonnen werden. Die Tumor-Organoide werden in immungeschwächte Mäuse implantiert, um sogenannte „Patient-Derived Orthotopic Xenografts“ (PDOXs, deutsch: „vom Patienten abgeleitete Xenotransplantate“) zu erzeugen. Bei einer Xenotransplantation handelt es sich um die Übertragung von lebens- und funktionstüchtigen Zellen oder Zellverbänden zwischen verschiedenen Spezies, in diesem Fall also von Mensch zu Maus.
Patienten-Avatare geben Merkmale der ursprünglichen Patiententumore sehr genau wieder
NORLUX verfügt derzeit über eine umfassende Kohorte von mehr als dieser 40 PDOX aus malignen Gliomen (bestimmte bösartige Hirntumore) einschließlich des Glioblastoms, einer der tödlichsten Formen des Hirnkrebs. Diese Modelle fungieren als klinisch relevante Patienten-„Avatare“, die die wichtigsten biologischen, histologischen und genomischen Merkmale der ursprünglichen Patiententumore sehr genau wiedergeben.
Die Kohorte umfasst Xenotransplantate von primären Gliomen und Ihren Rezidiven (Rückfälle) in verschiedenen Stadien, von verschiedenen Subtypen und mit verschiedenen genetischen Mutationen. Individuelle Xenotransplantate, die aus Tumorproben desselben Patienten vor und nach der Behandlung gewonnen werden, stehen ebenfalls zur Verfügung und verbessern das Verständnis dafür, wie bestimmte Krebsarten je nach ihren genetischen Eigenschaften auf verschiedene Behandlungen ansprechen.
Erfolgschancen klinischer Studien werden erhöht
Das neue Werkzeug ermöglicht personalisierte Studien zur Arzneimittelwirksamkeit. Dadurch können die Erfolgschancen klinischer Studien erhöht und klinische Forschungsergebnisse für die Patienten verbessert werden. „Hirntumor-Organoide und die daraus resultierenden Maus-Avatare haben einen einzigartigen Wert als Arzneimittel-Screening-Plattform sowohl in präklinischen als auch in behandlungsbegleitenden Studien“, erklärt Anna Golebiewska, Gruppenleiterin bei NORLUX und Co-Erstautorin der wissenschaftlichen Publikation. Konkret könnten sie im Rahmen der Präzisions-Onkologie eingesetzt werden, aber auch in weiteren Forschungsstudien in Kooperation mit pharmazeutischen Unternehmen. „Tatsächlich haben wir in unserer Studie die Wirksamkeit von VAL-083, einem Molekül von DelMar Pharmaceuticals, in unseren Organoiden und PDOXs getestet und gezeigt, dass es ein vielversprechender Kandidat zur Glioblastom-Behandlung ist”, so Anna Golebiewska.
„Unsere Arbeit ist das Ergebnis eines starken interdisziplinären Austauschs, der auf den komplementären Kompetenzen der biomedizinischen Forschung in Luxemburg basiert“, erklären dazu Ann-Christin Hau und Anaïs Oudin vom NORLUX-Forschungsteam und Co-Erstautoren der Publikation. „Wir sind überzeugt, dass unsere präklinischen Modelle die Umsetzung grundlegender Ergebnisse und Erkenntnisse in verbesserte klinische Behandlungen für zukünftige Patienten beschleunigen werden”, fügen sie hinzu.
Spürbare Erfolge in der personalisierten Krebstherapie
Die Sammlung von 40 PDOX-Glioma-Modellen und die zugehörigen Daten stehen der internationalen wissenschaftlichen Gemeinschaft auf PDXfinder, einem offenen globalen, von mehreren Instituten und Laboren entwickelten Katalog, zur Verfügung. „Durch die gemeinsame Nutzung unserer Modelle und Daten und durch die Zusammenarbeit mit führenden internationalen Partnern tragen wir kontinuierlich dazu bei, die Verfügbarkeit und Nutzung dieser unschätzbaren Ressourcen auf globaler Ebene zu erhöhen und unterstützen damit spürbar Erfolge in der personalisierten Krebstherapie“, meint auch Simone Niclou, Direktorin der LIH-Abteilung für Onkologie (DONC) und korrespondierende Autorin der Publikation.
Die Ergebnisse wurden im Oktober 2020 in der internationalen Zeitschrift Acta Neuropathologica veröffentlicht.
Autor: LIH
Editor: Uwe Hentschel






