LIH
Effekt der Blockade der Autophagie auf Tumouren
Wissenschaftler am LIH entdecken einen Mechanismus zur Hemmung von Hautkrebswachstum durch Erleichterung des Angriffs von „Natural Killer” Immunzellen.
Die Zellen mit dem gefährlich klingenden Namen „Natural Killer”, auch NK-Zellen oder natürliche Killerzellen genannt, sind Subpopulationen der weißen Blutkörperchen unseres Immunsystems und besitzen die Fähigkeit, abnormale Zellen einschließlich Krebszellen zu töten.
Die NK-Zellen spielen daher eine entscheidende Rolle bei der Immunreaktion gegen Tumoren. Die Krebszellen können jedoch diesen Abwehrmechanismus des Körpers unterbinden, indem sie sich mit einem Umfeld umgeben, das ein Eindringen der NK-Zellen verhindert und so das Krebswachstum ermöglicht.
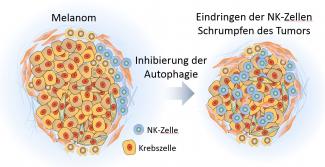
Bei der Erforschung des Melanoms, einer gefährlichen Form von Hautkrebs, hat das Forschungsteam von Dr. Bassam Janji am Luxembourg Institute of Health (LIH) einen Mechanismus aufgedeckt, der eine Umwandlung der direkten Umgebung des Tumors ermöglicht, so dass die NK-Zellen ins Innere des Tumors befördert werden, wo sie die Krebszellen angreifen und eine Rückbildung des Tumors bewirken können. Die Forscher sprechen von der Umwandlung eines immunosuppressiven in ein immunstimulierendes Tumor-Umfeld.
Diese Entdeckung wurde in der letzten Oktoberausgabe der angesehenen Fachzeitschrift „Proceedings of the National Academy of Sciences of the United States of America“ (PNAS) veröffentlicht. Ziel dieser Forschungen ist die Entwicklung neuer Strategien zur Immuntherapie, das heißt von Behandlungsmethoden zur Krebsbekämpfung durch Stärkung des Immunsystems.
Blockieren eines Zellprozesses
Bösartige Tumoren entwickeln raffinierte Mechanismen zur Umgehung des Immunsystems und somit zur Sicherung ihres Überlebens. Indem sie ihre Umgebung undurchdringlich für Immunzellen machen, verhindern sie das Eindringen der NK-Zellen in den Tumor.
Folglich besteht eine große Herausforderung im Bereich der Krebstherapie darin, Strategien zu entwickeln, die in der Lage sind, die tumorale Umgebung für Immunzellen zugänglich zu machen und diese angriffsbereiten Zellen zum Tumor hinzuleiten.
Vor einigen Jahren haben Forschungsteams, zu denen auch das Team von Dr. Janji gehört, entdeckt, dass das Tumorwachstum in den Krebszellen durch Blockieren der Autophagie maßgeblich verlangsamt und sogar gestoppt werden kann. Die Autophagie ist ein Prozess, der es den Zellen des Organismus ermöglicht, ihre beschädigten Proteine wiederzuverwerten.
In dieser neuen Studie zeigt das Team von Dr. Janji zum ersten Mal in Zellkulturexperimenten und in einem Mausmodell, dass Krebszellen, in denen die Autophagie genetisch blockiert wird, beginnen einen Botenstoff namens CCL5 zu erzeugen. CCL5 ist ein Protein aus der Familie der Zytokine, das in der Lage ist, NK-Zellen in den Tumor zu locken. Auf diese Weise werden im Tumor bei abwesender Autophagie massiv NK-Zellen rekrutiert, die die Krebszellen angreifen und so das Wachstum von Melanomen anhalten können.
Mit Hilfe von Tumorbiopsien von Hautkrebspatienten konnte das Team von Dr. Janji zeigen, dass eine Beziehung zwischen der Produktion des Zytokins CCL5 und dem Eindringen der NK-Zellen besteht. Je mehr CCL5 in den Biopsien messbar war, desto mehr NK-Zellen waren dort vorhanden. Die Forscher haben auch festgestellt, dass Patienten mit Melanom im Durchschnitt länger überlebt haben, wenn ihre Tumoren hohe Mengen an CCL5 enthielten.
Die Resultate der Tumorbiopsien sind ermutigend, aber stellen nur eine Korrelation (ein Zusammenhang) dar. Um einen direkten kausalen Link zwischen Autophagie-Blockade, CCL5-Produktion und Rekrutierung von NK-Zellen zum Tumor in Menschen zu beweisen, sind weitere Experimente nötig.
Eine Entdeckung mit therapeutischem Potenzial
Es handelt sich um die erste Studie, die einen mechanistischen Zusammenhang zwischen der Autophagie und der Rekrutierung von NK-Zellen aufzeigt. Dr. Janji sieht in dieser Entdeckung ein hohes therapeutisches Potenzial. „Das Blockieren der Autophagie in Krebszellen ist eine vielversprechende Strategie, um die Kraft des Immunsystems gegen den Krebs zu stärken”, erklärt er.
„Wir wissen jetzt, wie wir eine immunsuppressive Tumor-Umgebung in ein immunstimulierendes Umfeld verwandeln können, das es den Immunzellen ermöglicht, zum Tumor zu gelangen. Die NK-Zellen weisen ein hohes antitumorales Potenzial auf, das aber nur genutzt werden kann, wenn diese Zellen effektiv zum Tumor hingeleitet werden.”
Das Team von Dr. Janji beabsichtigt nun zu untersuchen, ob das Blockieren der Autophagie nicht nur das Eindringen der NK-Zellen verändert, sondern auch das anderer Immunzellentypen mit zytotoxischen Eigenschaften. Insgesamt, untersuchen die Forscher die Auswirkungen der Autophagieblockade auf die Immunlandschaft des Melanoms, um neue Strategien zur Immuntherapie in Verbindung mit Autophagie-Hemmern zu entwickeln.
Forschungszusammenarbeit und Finanzierung
Das Forschungsprojekt wurde von den Mitgliedern der Forschungseinheit „Laboratory of Experimental Cancer Research” des „Department of Oncology” am LIH unter der gemeinsamen Leitung von Dr. Guy Berchem und Dr. Bassam Janji durchgeführt. Die Gruppe hat dafür eng mit anderen luxemburgischen und internationalen Forschungsgruppen zusammengearbeitet: „National Cytometry Platform“, „Department of Infection and Immunity“, LIH; „Life Sciences Research Unit“, Universität Luxemburg; „Laboratoire national de santé“; „Centre Hospitalier de Luxembourg“; INSERM UMR 981 und 1186, „Gustave Roussy Cancer Center“, Villejuif, Frankreich; und Universitätsklinikum Besançon, Frankreich.
Großzügig unterstützt wurden die Forschungsarbeiten vom „Fonds National de la Recherche“ (FNR), vom „FRS-FNRS-Télévie“, der „Fondation Cancer Luxembourg“, der „Fondation Calouste Gulbenkian“, der „Ligue contre le Cancer“ und dem „Institut National du Cancer“ in Frankreich sowie durch interne Finanzierungen.
Autor: LIH
Editor: Michèle Weber (FNR)
Bild: LIH
Referenz
Mgrditchian et al., 2017 “Targeting autophagy inhibits melanoma growth by enhancing NK cells infiltration in a CCL5-dependent manner”.
http://www.pnas.org/content/114/44/E9271.long
Infobox
Dr. Bassam Janji
Stellvertretender Leiter des “Laboratory of Experimental Cancer Research”
Department of Oncology
Luxembourg Institute of Health
E-mail: bassam.janji@lih.lu
Verfügbarkeit für Interviews: auf Anfrage bei der Kommunikationsabteilung
Juliette Pertuy
Kommunikationsbeauftragte
Luxembourg Institute of Health
Tel: +352 26970-893
E-mail: juliette.pertuy@lih.lu
Dr Malou Fraiture
Scientific writer
Luxembourg Institute of Health
Tel: +352 26970-895
E-mail: malou.fraiture@lih.lu







