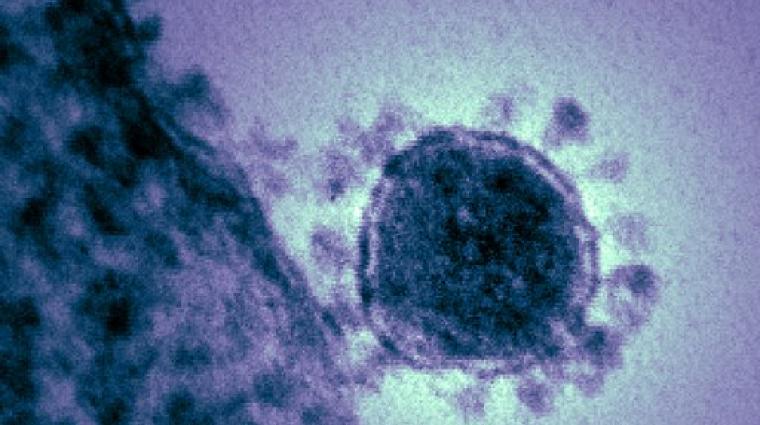
shotshop.com
Il n'est pas encore exactement clair comment le coronavirus est transmis d'une personne à l'autre.
Les experts soupçonnent que la première personne infecté avec le nouveau coronavirus 2019-nCoV l’a contracté dans un marché aux poissons de la ville chinoise de Wuhan, à travers un contact avec un animal infecté.
Comment un nouveau virus émerge-t-il chez l’homme? Qu’est-ce qui rend un virus dangereux pour l’homme? Et pourquoi de nouveaux virus continuent-ils d’apparaître chez l’homme? Explications par Dr Chantal Snoeck, qui est virologue au sein du Luxembourg Institute of Health et qui travaille, entre autres, sue les maladies appelées zoonotiques (qui se transmettent de l’animal à l’homme ou vice-versa) telles que la grippe aviaire et porcine.
Dr Snoeck, comment un nouveau virus émerge-t-il chez l’homme ?
CS : Une large proportion (approx. 60%) des maladies infectieuses humaines sont ce que l’on appelle des zoonoses, càd d’origine animale et transmises à l’homme. Ces virus zoonotiques proviennent majoritairement d’autres mammifères, mais les oiseaux sont aussi des hôtes de virus transmissibles à l’homme, comme certaines souches du virus de la grippe aviaire.
Un concept pour illustrer le phénomène d’émergence est « la pyramide des pathogènes ». L’émergence d’un virus dépend tout d’abord du degré d’exposition de la population humaine (niveau 1), par exemple par contact direct avec des animaux ou leurs excrétions (matières fécales, sang, salive,…), par l’alimentation ou l’eau contaminée, par l’intermédiaire d’un vecteur (tiques, moustiques,…). Bien que l’homme soit en contact permanent avec de nombreux pathogènes, tous ne sont pas capables d’infecter l’homme en raison de la barrière d’espèce, càd la capacité du virus à infecter une cellule du corps humain (niveau 2). Ensuite, une proportion de ces virus sont capables de se transmettre d’un homme à l’autre de manière limitée (niveau 3) ou non (niveau 4).
La capacité d’un virus à passer d’un niveau à l’autre dépend de caractéristiques intrinsèques du virus lui-même mais également de l’hôte qu’il rencontre. Une personne immunodéprimée est potentiellement plus à risque d’être infectée.
On lit souvent que les virus, y compris le coronavirus, peuvent changer par mutation rapidement. Est-ce que c’est également un façon d’évoluer d’un hôte à un autre ?
CS : Oui, un virus peut également évoluer au cours du temps grâces à des mécanismes comme la mutation, un changement dans la séquence génétique. Par exemple, dans le cas des virus de la grippe, certaines mutations permettent à un virus circulant chez les oiseaux d’augmenter son affinité pour les récepteurs cellulaires mammifères ou pour une réplication accrue dans les cellules de mammifères par rapport aux cellules aviaires.
Un virus existe dans son hôte comme une population de virus tous légèrement différents les uns des autres.
Infobox
Le concept de « quasi-espèce » virale stipule qu’un virus existe dans son hôte comme une population de virus tous légèrement différents les uns des autres. En conséquence, c’est aussi une population de particules virales qui infecte un hôte. Quand un facteur externe change, par exemple des particules virales du virus de la grippe aviaire a réussi à infecter une cellule humaine, la pression de sélection change et va influencer quelles particules vont se répliquer de manière plus efficace et générer la majorité de la descendance. Cette descendance, légèrement différente de la population parentale initiale, va pouvoir infecter l’hôte suivant. La présence d’une mutation particulière, comme celles qui augmentent l’affinité pour un récepteur cellulaire donné, donne un avantage (appelé « increased fitness ») à ces particules virales qui vont dès lors dominer la nouvelle population virale.
Cette diversité de la population virale se créée lors de sa réplication : lorsque le virus se multiple dans une cellule, il doit copier son matériel génétique et il ne le fait pas toujours de manière fidèle. Des erreurs, les mutations, peuvent être introduites dans le nouveau génome recopié. Ce phénomène est plus fréquent chez les virus dont la matériel génétique est de l’ARN comparé aux virus dont le matériel génétique est de l’ADN.
La recombinaison (l’échange de gène ou de portion de gène) ou le réassortiment de gène (pour les virus à génome segmenté) sont d’autres mécanismes qui permettent l’évolution des virus.
Qu’est-ce qui rend un virus dangereux pour l’homme?
CS : La dangerosité d’un agent pathogène provient de la combinaison de deux facteurs : la facilité avec laquelle il se transmet de l’homme à l’homme (R0) et la gravité des symptômes qu’il provoque (soit le taux de mortalité chez les personnes infectées), et il existe un continuum de R0 et de virulence.
Qu’est-ce que cela veut dire ?
Le R0, le nombre de reproduction de base, indique combien de personnes sont infectées par une personne contaminée, et donne donc une indication à quel point le nouveau virus est contagieux. Un R0 élevé indique qu’un virus se transmet facilement d’une personne à l’autre.
La rougeole est considérée comme une des maladies les plus contagieuses, avec un R0 entre 12 et 18 souvent cité (mais les estimations varient entre études). Un R0 élevé a des conséquences directes sur les stratégies de prévention : une couverture vaccinale de la population de 95% doit être atteint pour enrayer la propagation du virus de la rougeole. En comparaison, le virus de la rage se propage rarement entre deux personnes, les cas humains sont majoritairement liés à une source d’origine animale.
Le R0 est estimé avec des modèles mathématiques complexes, prenant en compte de nombreux facteurs tels que la transmissibilité du virus, le nombre de personnes avec lesquelles une personne infectée est entrée en contact et la durée pendant laquelle une personne infectée est contagieuse. Plus la connaissance du virus est grande, meilleure sera l’estimation de ce R0.
La virulence est la capacité d’un agent infectieux à causer une maladie. Plus la virulence est grande, plus les conséquences pour l’hôte infecté sont importantes. Certains virus peuvent infecter un hôte sans l’apparition de symptômes, y compris l’homme, alors que d’autres engendrent quasi systématiquement la mort, comme c’est le cas pour le virus de la rage.
Un virus qui ne se transmet pas facilement mais qui cause une taux de mortalité élevé peut atteindre le même niveau de dangerosité qu’un virus qui se transmet facilement avec un taux de mortalité plus faible.
À l’heure actuelle, que sait-on sur la R0 et le taux de mortalité du nouveau coronavirus ?
CS : Dans le cas du 2019-nCoV, une première estimation du R0 a été déjà été faite par plusieurs équipes indépendantes qui l’estiment entre 1.4 et 3.8. Cela veut dire qu’en moyenne, une personne infectée va passer le virus à 1 à 3 personnes supplémentaires.
Selon le ECDC, il y a 6057 cas confirmés et 132 décès (état de situation au 29.01.2020). Cela indique un taux de mortalité entre 2 et 3 % actuellement. Pour mettre cela dans un contexte : entre 291.000 et 646.000 personnes dans le monde meurent chaque année des suites d’une maladie respiratoire liée à la grippe saisonnière, causée par le virus de la grippe Influenza. On estime que ces épidémies annuelles entraînent environ 3 à 5 millions de cas de maladies graves par année.
SARS, MERS, Zika, Ebola…Coronavirus…le nombre d’épidémies causés par des virus semble augmenter au cours des dernières décennies ? Vrai ou faux ?
CS : Des outils de modélisation suggèrent en effet que la fréquence des épidémies augmente considérablement, y compris celles d'origine zoonotique. Selon cette étude, les auteurs estiment que le nombre d’épidémies d’origine zoonotique a plus que triplé entre 1980 et 2010 (de moins de 500 à plus de 1500 à l’échelle mondiale).
Pourquoi de nouveaux virus continuent-ils d'apparaître?
CS : L’émergence d’un nouveau virus désigne l’apparition d’un virus qui n’était pas encore connu ou une infection déjà connue mais qui se propage dans un nouvel hôte ou une répartition géographique beaucoup plus vaste. C’est par exemple le cas du virus Zika qui a été découvert en 1947 mais qui s’est propagé de manière exponentielle en Polynésie française en 2013-2014 puis en Amérique du Sud et latine en 2015-2016 en causant de larges épidémies et les cas assez médiatisés de microcéphalie chez les nouveaux-nés.
En plus de ceux cités précédemment liés au virus lui-même (mutation, échange de matériel génétique), de nombreux facteurs influencent l’émergence d’un nouveau virus (Howard and Fletcher, 2012) :
- Le changement climatique, particulièrement pour les maladies transmises par des vecteurs tels que les tiques ou les moustiques
- L’augmentation du contact direct et indirect entre la faune sauvage et domestique et la faune sauvage et l’homme par la déforestation, l’augmentation de la surface agricole, l’essor de l’élevage à l’échelle mondiale, le commerce et la consommation de viande exotique/faune sauvage
- L’augmentation de la taille de population mondiale, la concentration urbaine
- L’augmentation des mouvements d'animaux et de produits d'origine animale
- La fréquence et vitesse des déplacements locaux et internationaux
- Les comportements humains tels des changements d’habitudes alimentaires ou la popularité des animaux de compagnie exotiques
- Une augmentation de l’espérance de vie (plus de personnes âgées avec un système immunitaire moins efficace qu’une personne jeune) et de la population avec un système immunitaire compromis
- Mais aussi, notre capacité a détecté plus facilement et rapidement l’émergence d’un nouveau pathogène par une surveillance accrue, une amélioration constante des systèmes de soins de santé et le partage d’information au niveau international.
Dr Snoeck, un Grand Merci pour ces précisions très détaillées !
Chantal Snoeck est virologue au sein du l’équipe de virologie clinique et appliquée, dans le département infection et immunité au LIH. Les activités du groupe comprennent la surveillance, le diagnostic, les enquêtes sur les épidémies, l'épidémiologie moléculaire et l'immunité contre diverses maladies virales telles que la rougeole. Les informations sur la prévalence, la variabilité, la pathogénicité des virus et le degré d’immunité de la population sont importantes pour les décideurs en santé publique pour contrôler et gérer les maladies infectieuses. Chantal Snoeck travaille plus particulièrement sur les maladies virales zoonotiques telles que la grippe aviaire et porcine, le virus de l’hépatite E, ainsi que les maladies animales virales à forte conséquence économique.
Texte: Chantal Snoeck (LIH)
Questions et édition: Michèle Weber (FNR)
Graphique basé sur les statistiques publiées ici.