FNR
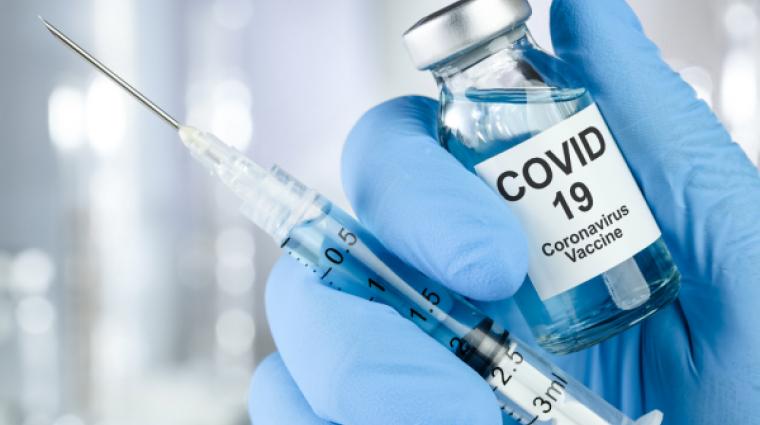
Zu den mRNA-Impfstoffen zählen Biontech/Pfizer, Moderna und CureVac.
Eine Einschätzung von Dr. Gérard Schockmel zu den Corona-mRNA-Impfstoffen gibt es am Ende des Artikels.
Biontech/Pfizer
- Name: Comirnaty, Tozinameran, BNT162b2
- Hersteller: Biontech/Pfizer
- Land: Deutschland / USA
- Impfstoff-Plattform: mRNA
- Impfregime: 2 Impfungen, Zweitimpfung soll nach 21 Tagen erfolgen, (28 Tage lt. CDC)
- Wirksamkeit (Studie): 95%, 100 % gegen schwere Verläufe
- Wirksamkeit (Feld): 94% - 99,9%
- Zugelassen / empfohlen für: ab 16 Jahre
- Bestellte Impfdosen für Luxemburg: für 337.645 Personen
Inhaltsstoffe
1 Dosis (0,3 ml) enthält:
30 Mikrogramm Messenger-RNA (mRNA) (eingebettet in Lipid-Nanopartikel)
Wirkweise
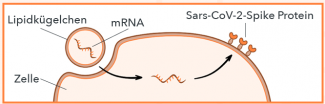
Der Impfstoff besteht aus Lipidkügelchen, welche mRNA enthalten. Diese mRNA ist der Bauplan für das Sars-CoV-2-Spike Protein. Die Lipidkügelchen bringen die mRNA in unsere Zellen. Die Zellen lesen die mRNA und stellen das Sars-CoV-2-Spike Protein her. Unser Immunsystem erkennt den Fremdkörper und kann passende Antikörper produzieren. Ist dieser Prozess abgeschlossen, ist Impfschutz vorhanden: Kommt unser Körper nun mit Sars-CoV-2-Viren in Kontakt, erkennt unser Immunsystem diese schnell und leitet sofort die erlernte Abwehrreaktion ein. Dadurch sinkt die Wahrscheinlichkeit (je nach Wirksamkeit des Impfstoffs), dass Geimpfte an Covid-19 erkranken. Vor allem bietet die Impfung einen guten Schutz gegen schwere Verläufe von Covid-19.
Infobox
- hohe Wirksamkeit (siehe Text)
- schnell herzustellen
- schnell an neue Virusvarianten anzupassen
- keine giftigen oder tierischen Materialien aus der Herstellung
- "Minimal-Vektor" (siehe Text)
- sind nicht infektiös
- vergleichsweise teuer
- nur bei tiefen Temperaturen lagerbar
- fehlende Langzeit-Erfahrung mit dieser Impfstoffgruppe
- keine schwerwiegenden Nebenwirkungen
- häufig leichte Nebenwirkungen wie:
- Schmerzen an der Injektionsstelle (> 80 %)
- Müdigkeit (> 60 %)
- Kopfschmerzen (> 50 %)
- Muskelschmerzen (> 30 %)
- Schüttelfrost (> 30 %)
- Gelenkschmerzen (> 20 %)
- Fieber (> 10 %)
- Schwellung an der Injektionsstelle (> 10 %)
Während der bisherigen Impfkampagnen sind keine neuen, schwerwiegenden Nebenwirkungen bekannt geworden.
bei -70 °C für 6 Monate
bei -25 °C bis -15 °C für 2 Wochen (02/2021)
12€
- Entwicklung gestartet: 15/01/2020
- Phase 1 Studie begonnen: 22.04.2020 (Phase 1/2)
- Phase 3 Studie begonnen: 27.07.2020 (USA, Brasilien, Argentinien)
- Zulassungsprozess begonnen:
USA: 20.11.2020 (Antrag auf Notfallgenehmigung)
EU: 06.10.2020 (Rolling Review)
EU: 30.11.2020 (Antrag auf bedingte Marktzulassung) - Zulassung erhalten:
UK: 02.12.2020 (vorläufige Notfallverwendung)
USA: 11.12.2020 (Notfallverwendung)
EU: 21.12.2020 (bedingte Marktzulassung)

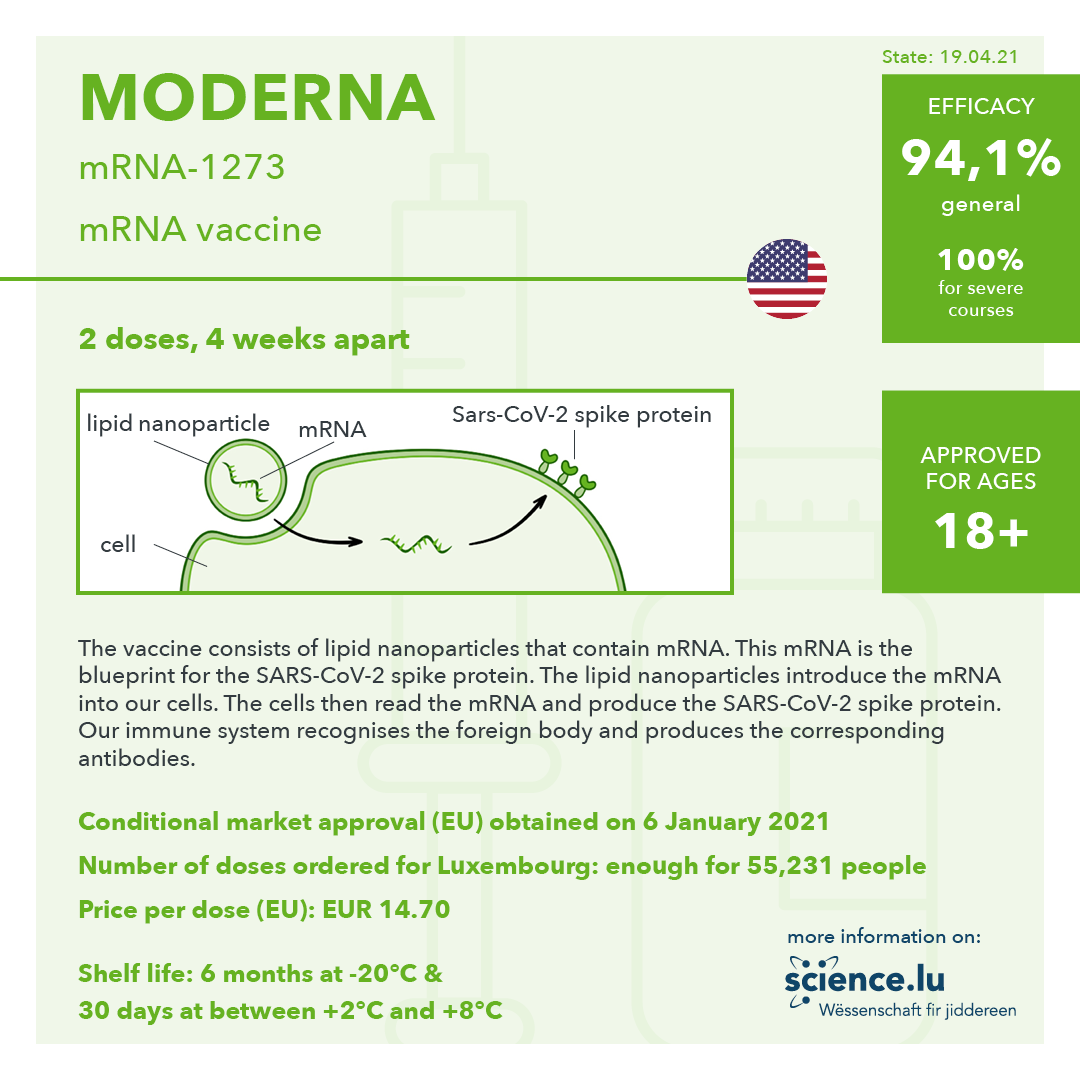
- Name: mRNA-1273
- Hersteller: Moderna
- Land: USA
- Impfstoff-Plattform: mRNA
- Impfregime: 2 Impfungen, Zweitimpfung soll nach 28 Tagen erfolgen
- Wirksamkeit (Studie): 94,1%, 100 % gegen schwere Verläufe
- Zugelassen / empfohlen für: ab 18 Jahre
- Bestellte Impfdosen für Luxemburg: für 55.231 Personen
Inhaltsstoffe
1 Dosis (0,5 ml) enthält:
100 Mikrogramm Messenger-RNA (mRNA) (eingebettet in Lipid-Nanopartikel)
Wirkweise
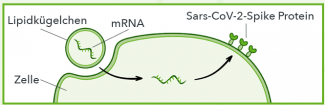
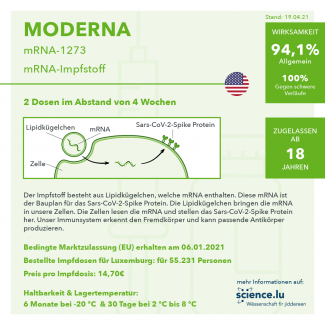
Der Impfstoff besteht aus Lipidkügelchen, welche mRNA enthalten. Diese mRNA ist der Bauplan für das Sars-CoV-2-Spike Protein. Die Lipidkügelchen bringen die mRNA in unsere Zellen. Die Zellen lesen die mRNA und stellen das Sars-CoV-2-Spike Protein her. Unser Immunsystem erkennt den Fremdkörper und kann passende Antikörper produzieren. Ist dieser Prozess abgeschlossen, ist Impfschutz vorhanden: Kommt unser Körper nun mit Sars-CoV-2-Viren in Kontakt, erkennt unser Immunsystem diese schnell und leitet sofort die erlernte Abwehrreaktion ein. Dadurch sinkt die Wahrscheinlichkeit (je nach Wirksamkeit des Impfstoffs), dass Geimpfte an Covid-19 erkranken. Vor allem bietet die Impfung einen guten Schutz gegen schwere Verläufe von Covid-19.
Infobox
- hohe Wirksamkeit (siehe Text)
- schnell herzustellen
- schnell an neue Virusvarianten anzupassen
- keine giftigen oder tierischen Materialien aus der Herstellung
- "Minimal-Vektor" (siehe Text)
- sind nicht infektiös
- vergleichsweise teuer
- nur bei tiefen Temperaturen lagerbar
- fehlende Langzeit-Erfahrung mit dieser Impfstoffgruppe
- Entwicklung gestartet: Januar 2020
- Phase 1 Studie begonnen: 04.03.2020 (Phase 1)
- Phase 3 Studie begonnen: 27.07.2020 (USA)
- Zulassungsprozess begonnen:
USA: 30.11.2020
EU: 16.11.2020 (Rolling Review)
EU: 30.11.2020 - Zulassung erhalten:
USA: 18.12.2020
EU: 06.01.2021
- keine schwerwiegenden Nebenwirkungen
- häufig leichte bis mittelschwere Nebenwirkungen wie:
- Schmerzen an der Injektionsstelle (92 %)
- Müdigkeit (70 %)
- Kopfschmerzen (64,7 %)
- Muskelschmerzen (61,5 %)
- Gelenkschmerzen (46,4 %)
- Schüttelfrost (45,4 %)
- Übelkeit/Erbrechen (23 %)
- Schwellung/Schmerzempfindlichkeit der axillären Lymphknoten (19,8 %)
- Fieber (15,5 %)
- Schwellung an der Injektionsstelle (14,7 %)
- Rötung an der Injektionsstelle (10 %)
- etwas häufiger bei jüngeren als bei älteren Probanden
- nach der zweiten Dosis häufiger als nach der ersten
Während der bisherigen Impfkampagnen sind keine neuen, schwerwiegenden Nebenwirkungen bekannt geworden.
14,70€
im Kühlschrank (2 bis 8 °C) für 30 Tage
bei -20 °C für 6 Monate
Quellen/nützliche Links
- Webseite des Herstellers
- Datenblatt / Produktinfo der EMA
- Datenblatt / Produktinfo des CDC
- Paper zur Phase 3 Studie
Einschätzung von Dr. Gérard Schockmel, Infektiologe an den "Hôpitaux Robert Schuman" (Stand 19. April 2021, Update 28 April 2021)

„Ein Vorteil der beiden derzeit zugelassenen mRNA-Impfstoffe ist ihr einfaches Design. Sie bestehen aus mRNA (als Bauplan zur Herstellung des Sars-CoV-2-Spike-Proteins), die in Lipid-Nanopartikel eingeschlossen ist – mehr nicht. Im Gegensatz zu den Vektorimpfstoffen enthalten sie keine Vektorviren.
Bei den mRNA-Impfstoffen treten stärkere Impfreaktionen in der Regel nach der zweiten Impfdosis auf. Bei dem Vektorimpfstoff von AstraZeneca hingegen ist es umgekehrt: stärkere Impfreaktionen treten nach der ersten Impfdosis auf, die zweite Impfdosis wird in der Regel deutlich besser vertragen.
Nach abgeschlossener Grundimmunisierung, d.h. ca. zwei Wochen nach der 2. Impfdosis erreichen die beiden RNA-Impfstoffe eine sehr hohe Wirksamkeit. Eine bereits recht hohe, partielle Wirksamkeit ist oftmals schon ca. 2-3 Wochen nach der 1. Impfdosis zu beobachten.
Das Sicherheitsprofil der beiden mRNA-Impfstoffe, die weltweit bereits an Millionen Menschen verabreicht wurden, ist ausgezeichnet. Dies erklärt den guten Ruf, den diese Impfstoffe derzeit in der Bevölkerung genießen. Der Moderna-Impfstoff besitzt überdies aufgrund seiner spezifischen Zusammensetzung gegenüber dem Pfizer/BioNTech-Impfstoff den Vorteil, dass er bei höheren Temperaturen gelagert werden kann – was die Vertriebslogistik erleichtert. Ansonsten ähneln sich die beiden mRNA-Impfstoffe sehr.
In sogenannten Virusneutralisationstests wurden die beiden mRNA-Impfstoffe gegen die derzeit zirkulierenden britische, südafrikanische und kalifornische Virusvarianten getestet. Beide mRNA-Impfstoffe zeigten eine ausgezeichnete Wirksamkeit gegen die britische und die kalifornische Virusvarianten.
Lediglich bei der südafrikanischen Variante war die Aktivität der neutralisierenden Antikörper deutlich herabgesetzt. Eine Möglichkeit diesem Aktivitätsverlust zu begegnen besteht theoretisch in der Verabreichung einer zusätzlichen, dritten Impfdosis desselben mRNA-Impfstoffes, oder aber in der Verabreichung eines auf die südafrikanische Variante zugeschnittenen mRNA-Impfstoffes. Beide Möglichkeiten werden derzeit in klinischen Studien untersucht. Zahlreiche Experten gehen jedoch davon aus, dass das 2-Dosen-Regime der beiden aktuellen mRNA-Impfstoffe auch bei der derzeitigen südafrikanischen Variante gegen schwere Covid-19 Verläufe schützt. Außerdem gilt es zu bedenken, dass T-Zellen an andere Stellen am Coronavirus Spike-Protein binden als Antikörper und daher eine Antikörper Escape-Mutation (Fluchtmutation) unter Umständen keinen Einfluss auf das Bindungsverhalten der T-Zellen besitzt. Für die Beurteilung der klinischen Wirksamkeit der aktuellen mRNA-Impfstoffe gegenüber Virusvarianten bedarf es jedoch der entsprechenden Impfstudien.
Die aktuelle Datenlage ist ungenügend, um die klinische Wirksamkeit der mRNA-Impfstoffe gegen die brasilianische Virusvariante zu beurteilen.
Insgesamt betrachtet stellt die mRNA-Technologie in meinen Augen einen medizinischen Quantensprung in der Entwicklung von genbasierten Impfstoffen dar. Die Herstellung der mRNA-Impfstoffe ist verhältnismäßig einfach. Das Design eines neuen mRNA-Impfstoffs ist innerhalb weniger Tage möglich, wenn man genau weiß, welche genetische Information gebraucht wird. Eben diese Anpassungsfähigkeit ist in der aktuellen epidemiologischen Situation sehr wichtig, da es produktionstechnisch erlaubt die mRNA-Impfstoffe an neu auftretende Virusvarianten anzupassen. Die Produktion von mRNA-Impfstoffen geht zudem schneller als dies bei herkömmlichen Impfstoffen der Fall ist und die mRNA-Impfstoffe sind, wie bereits oben erwähnt, virusfrei. Zudem bietet die mRNA-Technologie eine ganze Reihe neuer Möglichkeiten.“
Autoren der Serie: Kai Dürfeld (ScienceRELATIONS - Wissenschaftskommunikation), Jean-Paul Bertemes (FNR)
Illustrationen: Linda Wampach (FNR)
Steckbriefe: 101 Studios, Jean-Paul Bertemes (FNR)
Editoren: Michèle Weber (FNR), Melanie Reuter (FNR)